题目内容
【题目】已知:①2C(s)+O2(g)=2CO(g)ΔH=-220kJ·mol-1
②氢气燃烧的能量变化示意图:
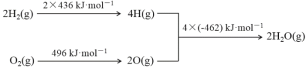
下列说法正确的是
A.1molC(s)完全燃烧放出110kJ的热量
B.C(s)+H2O(g)===CO(g)+H2(g)ΔH=+130kJ·mol-1
C.H2(g)+1/2O2(g)===H2O(g)ΔH=-480kJ·mol-1
D.欲分解2molH2O(l),至少需要提供4×462kJ的热量
【答案】B
【解析】
试题分析:A.1molC(s)完全燃烧生成1mol二氧化碳气体,放出的热量大于110 kJ,A错误;B.已知:①2C(s)+O2(g)═2CO(g)△H=-220kJmol-1,②H2(g)+1/2O2(g)═H2O(g)△H=-240kJmol-1,根据盖斯定律可知①×1/2-②得C(s)+H2O(g)═CO(g)+H2(g)△H=+130 kJmol-1,B正确;C.H2(g)+1/2O2(g)═H2O(g)△H=(436kJmol-1+1/2×496kJmol-1)-2×(462kJmol-1)=-240kJmol-1,C错误;D.由示意图可知,欲分解2 mol H2O(g),至少需要提供4×462 kJ的热量,D错误;答案选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目