题目内容
用下列实验装置进行相应实验,能达到实验目的的是( )。
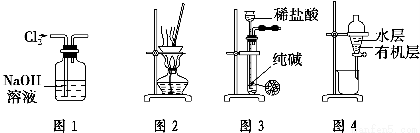
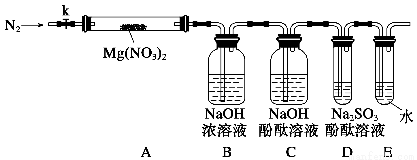
A.用图1所示装置除去Cl2中含有的少量HCl
B.用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.用图3所示装置制取少量纯净的CO2气体
D.用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层
D
【解析】NaOH溶液也能吸收Cl2,A项错误;加热NH4Cl易分解成NH3和HCl,B项错误;纯碱是细小的粉末,会漏下去的,同时制取的CO2中混有HCl和H2O,C项错误;I2在CCl4中的溶解度大且CCl4的密度大于水的密度,CCl4和水互不相溶,D项正确。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目