��Ŀ����
����Ŀ��ij��ȤС��������װ���о�ԭ��ص�ԭ����
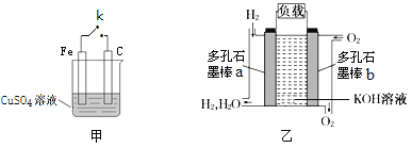
��1��װ�ü��k�Ͽ�ʱ��װ���з�����Ӧ�����ӷ���ʽΪ___�����k�պ�ʱ��C���ϵ�����Ϊ___���缫��ӦʽΪ___��
��2��װ����������ȼ�ϵ�ع���ʾ��ͼ������ͨ��������һ��Ϊ��ص�___�������������������������缫��ӦʽΪ___��
��3�����й���װ������ԭ��ص��ܷ�Ӧ��˵����ȷ����___����ѡ����ĸ����
A.�÷�Ӧ���ڷ�Ӧ��������С���������������ķ�Ӧ
B.�÷�Ӧ���ѻ�ѧ�����յ�������С���γɻ�ѧ���ͷŵ�������
C.�÷�Ӧ�����м��зǼ��Լ��Ķ������зǼ��Լ����γ�
���𰸡�Fe+Cu2+=Cu+Fe2+ ������ɫ���� Cu2++2e-=Cu �� H2+2e-+2OH-=2H2O B
��������
װ�ü��k�Ͽ�ʱ��ֱ�ӷ�����ѧ��Ӧ�����k�պ�ʱ������ԭ��ط�Ӧ��FeΪ������CΪ��������������ȼ�ϵ�أ�ͨ��ȼ�ϵ�Ϊ����������������Ӧ��ͨ��������Ϊ������������ԭ��Ӧ���ݴ˷����ش�
(1)װ�ü��k�Ͽ�ʱ��Fe��CuSO4��Һֱ�ӷ����û���Ӧ�����ӷ���ʽΪ��Fe+Cu2+=Cu+Fe2+�����k�պ�ʱ������ԭ��ط�Ӧ��CΪ�������缫��ӦʽΪ��Cu2++2e-=Cu���ڵ缫�����������ɫ���ʣ��ʴ�Ϊ��Fe+Cu2+=Cu+Fe2+��������ɫ���ʣ�Cu2++2e-=Cu��
(2)װ����������ȼ�ϵ�أ�ͨ��������һ��Ϊ��صĸ�����ʧ���ӷ���������Ӧ���������KOH��Һ��Ҫ���Ǻ�����Ӧ���ʸ�����ӦʽΪ��H2+2e-+2OH-=2H2O���ʴ�Ϊ������H2+2e-+2OH-=2H2O��
(3)A������ȼ�ϵ���ǽ�ȼ�շ�Ӧ�Ļ�ѧ��ת���ɵ��ܣ��ʷ�Ӧ����������������������������A����
B���÷�ӦΪ���ȷ�Ӧ���ʸ÷�Ӧ���ѻ�ѧ�����յ�������С���γɻ�ѧ���ͷŵ�����������B ��ȷ��
C���ܷ�Ӧ�ķ���ʽΪ��2H2+2O2=2H2O�����ѷǼ��Լ����γɵ��Ǽ��Լ�����C����
�ʴ�Ϊ��B��