题目内容
如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器。

其它条件相同时,在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):3X(g)+Y(g) 2 Z(g)。此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是( )
2 Z(g)。此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是( )

其它条件相同时,在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):3X(g)+Y(g)
 2 Z(g)。此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是( )
2 Z(g)。此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是( )| A.平衡时气体的平均摩尔质量:M(Ⅰ) <M(Ⅱ) |
| B.平衡时气体的密度:ρ(Ⅰ)>ρ(Ⅱ) |
| C.平衡时Ⅰ和Ⅱ中Z的百分含量z%(Ⅰ) > z% (Ⅱ) |
| D.平衡时气体的压强P(Ⅰ)<P (Ⅱ) |
BC
该反应是体积是减小的可逆反应,所以压强也是减小的,因此反应Ⅰ中的压强始终大于反应Ⅱ中的压强,D不正确。压强大,有利于平衡向正反应方向移动,即Ⅰ中反应物的转化率高,C正确。气体的总的物质的量少,混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,质量不变,所以M(Ⅰ)>M(Ⅱ),A不正确。密度是混合气的质量和容器容积的比值,在反应过程中质量是不变的,所以ρ(Ⅰ)>ρ(Ⅱ),C正确。答案选BC。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 bR(g)温度和压强对该反应的影响如图所示,其中压强p1<p2,由此可判断
bR(g)温度和压强对该反应的影响如图所示,其中压强p1<p2,由此可判断
 2Z(g),到达平衡后,Y的体积分数为a%,然后再向容器中通入2 mol Z,保持在恒温恒压下反应,当达到新的平衡时,Y的体积分数为b%。则a与b的关系是
2Z(g),到达平衡后,Y的体积分数为a%,然后再向容器中通入2 mol Z,保持在恒温恒压下反应,当达到新的平衡时,Y的体积分数为b%。则a与b的关系是 C(g)+2D(g)ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
C(g)+2D(g)ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是 ?pC(g)+qD(g)(如图)表示的是转化率与压强、温度的关系。分析图中曲线可以得出的结论是( )
?pC(g)+qD(g)(如图)表示的是转化率与压强、温度的关系。分析图中曲线可以得出的结论是( )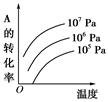
 pC(g),反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示压强不同的曲线,B图表示的是温度不同的曲线,试比较下列大小关系:P1______ P2, T1______ T2, ΔH_____ 0, a+b______ p。
pC(g),反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示压强不同的曲线,B图表示的是温度不同的曲线,试比较下列大小关系:P1______ P2, T1______ T2, ΔH_____ 0, a+b______ p。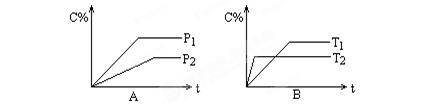
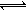 CO(g)+H2(g) △H=+131.3KJ.mol-1[各容器中C(s)均足量],在某时刻测得有关物质的浓度及正、逆反应速率的关系如下表。下列说法不正确的是
CO(g)+H2(g) △H=+131.3KJ.mol-1[各容器中C(s)均足量],在某时刻测得有关物质的浓度及正、逆反应速率的关系如下表。下列说法不正确的是