题目内容
锰的氧化物MnO2、Mn2O3、Mn3O4,Mn2O7在加热时均能和浓盐酸反应生成MnCl2和Cl2。现11.45 g锰的某种氧化物跟足量的盐酸反应,产生的氯气在标准状况下的体积为1.12 L,则参加反应的氧化物是( )
A.MnO2 B.Mn2O3 C.Mn3O4 D.Mn2O7
【答案】
C
【解析】设符合题意的锰的氧化物分子式为MnOx,在反应中Mn2x+得电子还原成Mn2+,化合价降低至+2价,得电子总数为(2x-2);Cl-在反应中失电子,化合价升高到0价,失电子总数为1,由关系式:
MnOx ~ (2x-2)Cl-
(55+16x)g (2x-2)mol
11.45 g 0.05×2 mol
(55+16x)︰11.45=(2x-2)︰0.1,解得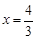 ,由
,由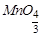 可推出该化合物为Mn3O4。
可推出该化合物为Mn3O4。

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目