题目内容
完成下列填空
(1)下列物质能导电的是
a.铜丝 b.金刚石 c.石墨 d.NaCl e.盐酸 f.蔗糖 g.CO2 h.Na2O i.硬脂酸 j.醋酸k.碳酸 l.碳酸氢铵 m.氢氧化铝 n.氯气 P BaSO4
(2)有氢离子浓度相同、体积相等的三种酸:a、盐酸 b、硫酸 c、醋酸,p同时加入足量的锌,则开始反应时速率
(3)物质的量浓度相同的盐酸、硫酸和醋酸溶液,pH最小的是
(4)已知1mol N2与适量 H2反应生成NH3放出92.2KJ热量.写出表示该反应的热化学方程式
(5)4.0g硫在氧气中完全燃烧放出37kJ热量,则硫的燃烧热为
(6)BaSO4(溶解平衡表达式)
(7)H2CO3(电离方程式)
(8)NH4Cl(水解离子方程式)
(9)NaHCO3溶液中存在那些微粒?
(1)下列物质能导电的是
acejk
acejk
,属于强电解质的是dhp
dhp
,属于弱电解质的是ijkm
ijkm
,属于非电解质的是fg
fg
.a.铜丝 b.金刚石 c.石墨 d.NaCl e.盐酸 f.蔗糖 g.CO2 h.Na2O i.硬脂酸 j.醋酸k.碳酸 l.碳酸氢铵 m.氢氧化铝 n.氯气 P BaSO4
(2)有氢离子浓度相同、体积相等的三种酸:a、盐酸 b、硫酸 c、醋酸,p同时加入足量的锌,则开始反应时速率
相同
相同
,反应完全后生成H2的质量a=b<c
a=b<c
.(用<、=、>表示)(3)物质的量浓度相同的盐酸、硫酸和醋酸溶液,pH最小的是
硫酸
硫酸
,pH最大的是醋酸
醋酸
;体积相同时分别与同种NaOH溶液反应,消耗NaOH溶液的体积大小关系为v硫酸=2v盐酸>2v醋酸
v硫酸=2v盐酸>2v醋酸
.(4)已知1mol N2与适量 H2反应生成NH3放出92.2KJ热量.写出表示该反应的热化学方程式
N2(g)+3H2(g) 2NH3(g)△H=-92kJ?mol-1
2NH3(g)△H=-92kJ?mol-1
 2NH3(g)△H=-92kJ?mol-1
2NH3(g)△H=-92kJ?mol-1N2(g)+3H2(g) 2NH3(g)△H=-92kJ?mol-1
2NH3(g)△H=-92kJ?mol-1
 2NH3(g)△H=-92kJ?mol-1
2NH3(g)△H=-92kJ?mol-1(5)4.0g硫在氧气中完全燃烧放出37kJ热量,则硫的燃烧热为
S(s)+O2(g)═SO2(g)△H=-296KJ/mol
S(s)+O2(g)═SO2(g)△H=-296KJ/mol
(6)BaSO4(溶解平衡表达式)
BaSO4(s) Ba2+(aq)+SO42-(aq)
Ba2+(aq)+SO42-(aq)
 Ba2+(aq)+SO42-(aq)
Ba2+(aq)+SO42-(aq)BaSO4(s) Ba2+(aq)+SO42-(aq)
Ba2+(aq)+SO42-(aq)
 Ba2+(aq)+SO42-(aq)
Ba2+(aq)+SO42-(aq)(7)H2CO3(电离方程式)
H2CO3 H++HCO3-
H++HCO3-
 H++HCO3-
H++HCO3-H2CO3 H++HCO3-
H++HCO3-
 H++HCO3-
H++HCO3-(8)NH4Cl(水解离子方程式)
NH4++H2O  H++NH3?H2O
H++NH3?H2O
 H++NH3?H2O
H++NH3?H2ONH4++H2O  H++NH3?H2O
H++NH3?H2O
 H++NH3?H2O
H++NH3?H2O(9)NaHCO3溶液中存在那些微粒?
两种分子(H2O、H2CO3)和五种离子(H+、Na+、OH-、CO32-、HCO3-)
两种分子(H2O、H2CO3)和五种离子(H+、Na+、OH-、CO32-、HCO3-)
.分析:(1)水溶液中或熔融状态下能够导电的化合物称为电解质,酸、碱、盐都是电解质;在上述两种情况下都不能导电的化合物称为非电解质,蔗糖、乙醇等都是非电解质.大多数的有机物都是非电解质;单质,混合物不管在水溶液中或熔融状态下能够导电与否,都不是电解质或非电解质.能导电的物质--必须具有能自由移动的带电的微粒,金属能导电--是由于金属中存在能自由移动的带负电的电子,强电解质是在水溶液中能完全电离的电解质,弱电解质是在水溶液里部分电离的电解质;
(2)化学反应速率与浓度成正比,考虑弱酸的部分电离;
(3)一分子硫酸能产生2个H+,盐酸只能产生一个H+;物质的量浓度相同,n(H+)硫酸是盐酸的两倍.
醋酸也能产生一个H+,但醋酸是弱酸,不能完全解离;
(4)根据热化学方程式的书写要求;
(5)根据热化学方程式的书写方法,注意燃烧热可燃物为1mol;
(6)根据溶解平衡方程式的书写方法;
(7)多元弱酸的电离以第一步为主;
(8)根据水解方程式的书写方法;
(9)在NaHCO3溶液中,NaHCO3完全电离出Na+和HCO3-,而HCO3-又能水解产生H2CO3和OH-,同时又能电离出H+和CO32-,再加上水电离出的H+和OH-.
(2)化学反应速率与浓度成正比,考虑弱酸的部分电离;
(3)一分子硫酸能产生2个H+,盐酸只能产生一个H+;物质的量浓度相同,n(H+)硫酸是盐酸的两倍.
醋酸也能产生一个H+,但醋酸是弱酸,不能完全解离;
(4)根据热化学方程式的书写要求;
(5)根据热化学方程式的书写方法,注意燃烧热可燃物为1mol;
(6)根据溶解平衡方程式的书写方法;
(7)多元弱酸的电离以第一步为主;
(8)根据水解方程式的书写方法;
(9)在NaHCO3溶液中,NaHCO3完全电离出Na+和HCO3-,而HCO3-又能水解产生H2CO3和OH-,同时又能电离出H+和CO32-,再加上水电离出的H+和OH-.
解答:解:(1)能导电的物质--必须具有能自由移动的带电的微粒,金属铜和石墨中存在能自由移动的带负电的电子能导电,盐酸醋酸碳酸中都有能自由移动的正负离子,也能导电;强电解质是在水溶液中能完全电离的电解质,NaCl、BaSO4在水溶液里完全电离,Na2O在熔融状态下完全电离;弱电解质是在水溶液里部分电离的电解质,硬脂酸、醋酸、碳酸、氢氧化铝在水溶液里部分电离;蔗糖在水溶液中或熔融状态下均不导电,二氧化碳的水溶液能导电,但不是它本身导电,属于非电解质,故答案为:acejk;dhp;ijkm;fg;
(2)化学反应速率与浓度成正比,开始时氢离子浓度相同,化学反应速率相同,盐酸和硫酸中氢离子的物质的量相等,生成的氢气相等,考虑弱酸的部分电离,醋酸的浓度比盐酸和硫酸的大,生成的氢气多,故答案为:相同;a=b<c;
(3)一分子硫酸能产生2个H+,盐酸只能产生一个H+;物质的量浓度相同,n(H+)硫酸是盐酸的两倍.
醋酸也能产生一个H+,但醋酸是弱酸,不能完全解离,也就是说醋酸的物质量要比盐酸的小,所以pH最小的是硫酸,pH最大的是醋酸,体积相同时分别与同种NaOH溶液反应,消耗NaOH溶液的体积大小关系为:v硫酸=2v盐酸>2v醋酸,
故答案为:硫酸;醋酸;v硫酸=2v盐酸>2v醋酸;
(4)热化学方程式为:N2(g)+3H2(g) 2NH3(g)△H=-92kJ?mol-1,
2NH3(g)△H=-92kJ?mol-1,
故答案为:N2(g)+3H2(g) 2NH3(g)△H=-92kJ?mol-1;
2NH3(g)△H=-92kJ?mol-1;
(5)4g硫粉完全燃烧生成二氧化硫气体,放出37kJ的热量,所以32g硫粉完全燃烧生成二氧化硫气体,放出296kJ的热量,则热化学方程式为:S(s)+O2(g) ═SO2(g) △H=-296KJ/mol,
故答案为:S(s)+O2(g)═SO2(g)△H=-296KJ/mol;
(6)硫酸钡溶解平衡方程式:BaSO4(s) Ba2+(aq)+SO42-(aq),
Ba2+(aq)+SO42-(aq),
故答案为:BaSO4(s) Ba2+(aq)+SO42-(aq);
Ba2+(aq)+SO42-(aq);
(7)H2CO3电离方程式:H2CO3 H++HCO3-,故答案为:H2CO3
H++HCO3-,故答案为:H2CO3 H++HCO3-;
H++HCO3-;
(8)NH4Cl水解方程式:NH4++H2O H++NH3?H2O,故答案为:NH4++H2O
H++NH3?H2O,故答案为:NH4++H2O  H++NH3?H2O;
H++NH3?H2O;
(9)在NaHCO3溶液中,NaHCO3完全电离出Na+和HCO3-,而HCO3-又能水解产生H2CO3和OH-,同时又能电离出H+和CO32-,再加上水电离出的H+和OH-.因此溶液中共有两种分子(H2O、H2CO3)和五种离子(H+、Na+、OH-、CO32-、HCO3-),
故答案为:两种分子(H2O、H2CO3)和五种离子(H+、Na+、OH-、CO32-、HCO3-).
(2)化学反应速率与浓度成正比,开始时氢离子浓度相同,化学反应速率相同,盐酸和硫酸中氢离子的物质的量相等,生成的氢气相等,考虑弱酸的部分电离,醋酸的浓度比盐酸和硫酸的大,生成的氢气多,故答案为:相同;a=b<c;
(3)一分子硫酸能产生2个H+,盐酸只能产生一个H+;物质的量浓度相同,n(H+)硫酸是盐酸的两倍.
醋酸也能产生一个H+,但醋酸是弱酸,不能完全解离,也就是说醋酸的物质量要比盐酸的小,所以pH最小的是硫酸,pH最大的是醋酸,体积相同时分别与同种NaOH溶液反应,消耗NaOH溶液的体积大小关系为:v硫酸=2v盐酸>2v醋酸,
故答案为:硫酸;醋酸;v硫酸=2v盐酸>2v醋酸;
(4)热化学方程式为:N2(g)+3H2(g)
 2NH3(g)△H=-92kJ?mol-1,
2NH3(g)△H=-92kJ?mol-1,故答案为:N2(g)+3H2(g)
 2NH3(g)△H=-92kJ?mol-1;
2NH3(g)△H=-92kJ?mol-1;(5)4g硫粉完全燃烧生成二氧化硫气体,放出37kJ的热量,所以32g硫粉完全燃烧生成二氧化硫气体,放出296kJ的热量,则热化学方程式为:S(s)+O2(g) ═SO2(g) △H=-296KJ/mol,
故答案为:S(s)+O2(g)═SO2(g)△H=-296KJ/mol;
(6)硫酸钡溶解平衡方程式:BaSO4(s)
 Ba2+(aq)+SO42-(aq),
Ba2+(aq)+SO42-(aq),故答案为:BaSO4(s)
 Ba2+(aq)+SO42-(aq);
Ba2+(aq)+SO42-(aq);(7)H2CO3电离方程式:H2CO3
 H++HCO3-,故答案为:H2CO3
H++HCO3-,故答案为:H2CO3 H++HCO3-;
H++HCO3-;(8)NH4Cl水解方程式:NH4++H2O
 H++NH3?H2O,故答案为:NH4++H2O
H++NH3?H2O,故答案为:NH4++H2O  H++NH3?H2O;
H++NH3?H2O;(9)在NaHCO3溶液中,NaHCO3完全电离出Na+和HCO3-,而HCO3-又能水解产生H2CO3和OH-,同时又能电离出H+和CO32-,再加上水电离出的H+和OH-.因此溶液中共有两种分子(H2O、H2CO3)和五种离子(H+、Na+、OH-、CO32-、HCO3-),
故答案为:两种分子(H2O、H2CO3)和五种离子(H+、Na+、OH-、CO32-、HCO3-).
点评:本题是一道综合题,难度适中,注意元素化合物知识的积累,(3)为学生解答中的易错点.

练习册系列答案
相关题目

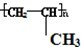

 ;若
;若 在上述类似条件下发生反应,请模仿上例写出该反应的方程式:
在上述类似条件下发生反应,请模仿上例写出该反应的方程式:



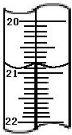 加碘食盐是在食盐中添加碘酸钾,当食盐含碘量(以I计算)超过20~50mg/kg,将对人体造成危害,所以检测食盐含碘量是保障加碘食盐质量的一项重要工作.某学生在实验室测定食用精制盐是否含碘及测定含碘量,主要反映为:
加碘食盐是在食盐中添加碘酸钾,当食盐含碘量(以I计算)超过20~50mg/kg,将对人体造成危害,所以检测食盐含碘量是保障加碘食盐质量的一项重要工作.某学生在实验室测定食用精制盐是否含碘及测定含碘量,主要反映为: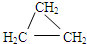 d.CH2=CHCH3.
d.CH2=CHCH3.