��Ŀ����
��ҵ���Ի�����Ϊԭ���������ᣬ������Ҫ��һ���Ǵ������������б��ֺ��º�����������2SO2��g����O2 ��g�� 2SO3��g�� ��H����196��6 kJ��mol��1
2SO3��g�� ��H����196��6 kJ��mol��1
��������Ϊ��߷�Ӧ���ʺ�SO2��ת���ʣ����д�ʩ���е���_______������ĸ����ͬ����
A����װ���г���N2
B����װ���г��������SO2
C����װ���г���O2
D�������¶�
������һ���¶��£���һ���ݻ��ɱ�ĺ�ѹ�����У�ͨ��3mol SO2 ��2mol O2 ���������������������Ӧ��ƽ��ʱ�������������Ϊ��ʼʱ��90%������ͬһ��Ӧ�¶ȣ�����ͬ�����У�����ʼ���ʵ�����Ϊ 5mol SO2��g����3��5 mol O2��g����1mol SO3��g�� ������˵����ȷ����___________
A����һ��ƽ��ʱ��Ӧ�ų�������Ϊ294��9kJ
B������ƽ��SO2��ת�������
C������ƽ��ʱ��O2����������
D���ڶ���ƽ��ʱSO3�������������2/9
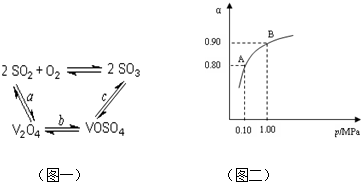
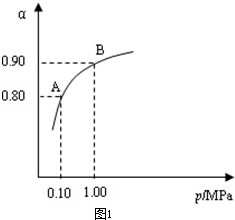
����������550 ��ʱ����2��0 mol SO2��1��0 mol O2���� 5 ���ܱ������У�SO2ת��ΪSO3��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ����Ӧ��ƽ�����ϵ��ѹǿΪ
0��10 M Pa���Լ��㷴Ӧ 2SO3 2SO2+O2 ��550 ��ʱ��ƽ�ⳣ��K=_________�� A��B��ʾ��ͬѹǿ�µ�ƽ��ת���ʣ�ͨ����ҵ�����в��ó�ѹ��ԭ���ǣ�__________________�����Ƚϲ�ͬѹǿ�µ�ƽ�ⳣ����K��0��10 MPa�� _________K��1��0 MPa������ ������������������
2SO2+O2 ��550 ��ʱ��ƽ�ⳣ��K=_________�� A��B��ʾ��ͬѹǿ�µ�ƽ��ת���ʣ�ͨ����ҵ�����в��ó�ѹ��ԭ���ǣ�__________________�����Ƚϲ�ͬѹǿ�µ�ƽ�ⳣ����K��0��10 MPa�� _________K��1��0 MPa������ ������������������
 2SO3��g�� ��H����196��6 kJ��mol��1
2SO3��g�� ��H����196��6 kJ��mol��1��������Ϊ��߷�Ӧ���ʺ�SO2��ת���ʣ����д�ʩ���е���_______������ĸ����ͬ����
A����װ���г���N2
B����װ���г��������SO2
C����װ���г���O2
D�������¶�
������һ���¶��£���һ���ݻ��ɱ�ĺ�ѹ�����У�ͨ��3mol SO2 ��2mol O2 ���������������������Ӧ��ƽ��ʱ�������������Ϊ��ʼʱ��90%������ͬһ��Ӧ�¶ȣ�����ͬ�����У�����ʼ���ʵ�����Ϊ 5mol SO2��g����3��5 mol O2��g����1mol SO3��g�� ������˵����ȷ����___________
A����һ��ƽ��ʱ��Ӧ�ų�������Ϊ294��9kJ
B������ƽ��SO2��ת�������
C������ƽ��ʱ��O2����������
D���ڶ���ƽ��ʱSO3�������������2/9
����������550 ��ʱ����2��0 mol SO2��1��0 mol O2���� 5 ���ܱ������У�SO2ת��ΪSO3��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ����Ӧ��ƽ�����ϵ��ѹǿΪ
0��10 M Pa���Լ��㷴Ӧ 2SO3
 2SO2+O2 ��550 ��ʱ��ƽ�ⳣ��K=_________�� A��B��ʾ��ͬѹǿ�µ�ƽ��ת���ʣ�ͨ����ҵ�����в��ó�ѹ��ԭ���ǣ�__________________�����Ƚϲ�ͬѹǿ�µ�ƽ�ⳣ����K��0��10 MPa�� _________K��1��0 MPa������ ������������������
2SO2+O2 ��550 ��ʱ��ƽ�ⳣ��K=_________�� A��B��ʾ��ͬѹǿ�µ�ƽ��ת���ʣ�ͨ����ҵ�����в��ó�ѹ��ԭ���ǣ�__________________�����Ƚϲ�ͬѹǿ�µ�ƽ�ⳣ����K��0��10 MPa�� _________K��1��0 MPa������ ������������������ 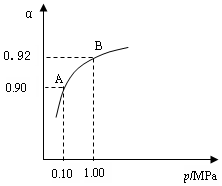
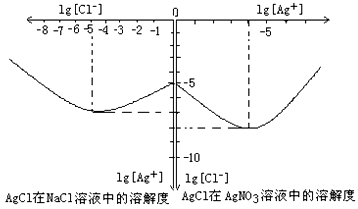
�ȳ����ﲢ�Ǿ��Բ��ܣ�����ˮ�����ֲ�ͬ����Һ���ܽ��������ͬ��ͬ����ЧӦ���������γɵȶ���ʹ��������ܽ�������ı䡣��֪AgCl + Cl- =[AgCl2]-����ͼ��ij�¶���AgCl��NaCl��Һ�е��ܽ��������������Ϣ��֪��
����ͼ֪���¶���AgCl���ܶȻ�����Ϊ__________________________��
��AgCl��NaCl��Һ�е��ܽ������ͼ��ʾ������ȱ�С����ԭ���ǣ�__________________________
����ͼ֪���¶���AgCl���ܶȻ�����Ϊ__________________________��
��AgCl��NaCl��Һ�е��ܽ������ͼ��ʾ������ȱ�С����ԭ���ǣ�__________________________
(1)C
(2)CD
(3)2.5��10-4����ѹ��400��500��C��SO2ת�����Ѿ��ܸ��ˣ���ѹ��������Ͷ���Խ�������豸���ṩ�������⣻=
(4) ��10-10���ڿ�ʼCl-������AgCl ���ܽ⣬����Ag+Ũ�ȱ�С�ˣ���Cl-Ũ������ʹAgCl �γ�[AgCl2]-��������Ag+Ũ���ֱ���ˡ�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
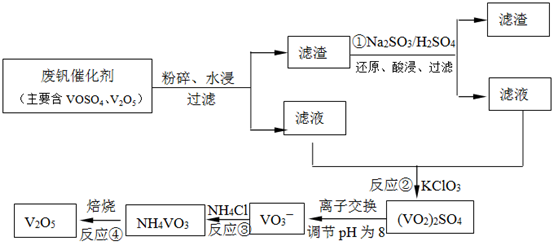
 ��ҵ���Ի�����Ϊԭ������������Ҫ��Ϊ�����ν��У������ա������������գ���ش����и����⣺
��ҵ���Ի�����Ϊԭ������������Ҫ��Ϊ�����ν��У������ա������������գ���ش����и����⣺