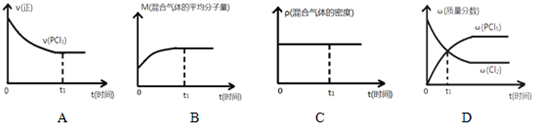
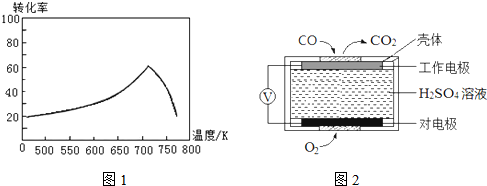
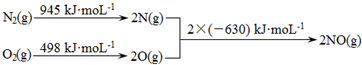题目内容
20.为了验证NaHCO3固体中是否含有Na2CO3,下列实验及判断中,正确的是( )| A. | 加热,观察是否有气体放出 | |
| B. | 加入盐酸,观察是否有气体放出 | |
| C. | 溶于水后加BaCl2溶液,观察有无沉淀出现 | |
| D. | 进行焰色反应,观察火焰是否呈黄色 |
分析 NaHCO3加热不稳定,易分解,Na2CO3和NaHCO3都可与酸、石灰水反应,都含有钠元素,焰色反应都呈黄色,以此解答该题.
解答 解:A.NaHCO3加热不稳定,易分解,生成气体,不能说明碳酸钠存在,故A错误;
B.Na2CO3和NaHCO3都可与盐酸反应生成气体,不能鉴别,故B错误;
C.Na2CO3和BaCl2溶液反应生成白色沉淀,而NaHCO3不能,能鉴别,故C正确;
D.都含有钠元素,焰色反应都呈黄色,不能鉴别,故D错误.
故选C.
点评 本题考查物质的检验和鉴别,为高频考点,注意把握性质的异同为解答该题的关键,学习中注意相关基础知识的积累,题目难度不大.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
5.下列说法正确的是( )
| A. | 液态 HCl、固体NaCl 均不导电,所以 HCl、NaCl 均是非电解质 | |
| B. | NH3、CO2的水溶液均导电,所以 NH3、CO2 均是电解质 | |
| C. | 铜、石墨均导电,所以它们是电解质 | |
| D. | 蔗糖、酒精在水溶液或熔化时均不导电,所以它们是非电解质 |
12.下列实验操作、现象和发生的离子反应完全正确的是( )
| 实验操作 | 现象 | 发生的离子反应 | |
| A | 向BaCl2 溶液中通入CO2 | 溶液浑浊 | Ba2++CO2+H2O═BaCO3↓+2H+ |
| B | 向NaAlO2溶液中滴加过量CO2 | 溶液浑浊 | AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
| C | 将可调高度的铜丝伸入到稀HNO3中 | 溶液变蓝 | Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
| D | 将Cl2通入KI溶液中,加入CCl4,振荡,静置 | 上层溶液显紫红色 | Cl2+2I-═2Cl-+I2 |
| A. | A | B. | B | C. | C | D. | D |
9.下列符合实际并用于工业生产的是( )
| A. | 电解氯化钠水溶液来制金属钠 | B. | 氢气和氯气混合后光照制氯化氢 | ||
| C. | 金属钠在氯气中燃烧制氯化钠 | D. | 氯气和石灰乳作用制漂白粉 |
10.澄清透明的溶液中能大量共存的是( )
| A. | Cu2+、C1-、SO42-、K+ | B. | K+、OH-、CO32-、Fe2+ | ||
| C. | Ca2+、OH-、C1-、Na+ | D. | Ag+、NO3-、Cl-、K+ |
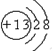 ,由A和B形成的含有非极性键的离子化合物的电子式是
,由A和B形成的含有非极性键的离子化合物的电子式是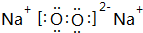 ;
;