题目内容
下列说法正确的是
| A.第三周期从左到右,各元素形成的简单离子半径逐渐减小 |
| B.共价化合物中一定含极性共价键,可能含非极性共价键 |
| C.第ⅦA族元素从上到下,其气态氢化物的稳定性和还原性均逐渐增强 |
| D.可能存在基态核外电子排布式为1s22s22p63s23p64s24p5的原子 |
B
试题分析:A、同一周期金属元素失去最外层电子形成阳离子,非金属得到电子形成阴离子,电子层数不变,故同周期阴离子半径大于阳离子半径,错误;B、共价化合物由多种元素组成,不同种元素形成极性共价键,故一定含极性共价键,可能含非极性共价键(如过氧化物),正确;C、第ⅦA族元素从上到下,元素非金属性逐渐减弱,故气态氢化物的稳定性逐渐减弱和还原性均逐渐增强,错误;D、基态原子中3d轨道能量比4p轨道低,应先排3d轨道后排4p轨道,错误。

练习册系列答案
相关题目
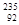 U是一种重要的核燃料,这里的“235”是指该原子的
U是一种重要的核燃料,这里的“235”是指该原子的