题目内容
(8分)20℃时,醋酸的电离平衡常数为1.6×10-5。
(1)试计算20℃时0.01mol?L-1的醋酸溶液中氢离子浓度。
(2)室温时,向0.2mol?L-1的醋酸溶液中加入等体积的0.1mol?L-1的NaOH(aq),充分反应后所得溶液的PH=4,则:
①所得溶液中各离子(包括CH3COOH分子)浓度大小关系是:______________________,
②所得溶液中的物料守恒式为:________+________=__________=_________mol?L-1。
③c(CH3COOH)=_____________mol?L-1(写出算式,不做近似计算)
(1)试计算20℃时0.01mol?L-1的醋酸溶液中氢离子浓度。
(2)室温时,向0.2mol?L-1的醋酸溶液中加入等体积的0.1mol?L-1的NaOH(aq),充分反应后所得溶液的PH=4,则:
①所得溶液中各离子(包括CH3COOH分子)浓度大小关系是:______________________,
②所得溶液中的物料守恒式为:________+________=__________=_________mol?L-1。
③c(CH3COOH)=_____________mol?L-1(写出算式,不做近似计算)
(8分)(1)4×10-4mol?L-1
(2)①c(CH3COO-) >c(Na+)>c(CH3COOH)>c(H+)>c(OH-)
>c(Na+)>c(CH3COOH)>c(H+)>c(OH-)
②c(CH3COO-)+c(CH3COOH)=2c(Na+)=0.1mol?L-1
③c(CH3COOH)=0.05-10-4+10-10mol?L-1(各2分)
(2)①c(CH3COO-)
 >c(Na+)>c(CH3COOH)>c(H+)>c(OH-)
>c(Na+)>c(CH3COOH)>c(H+)>c(OH-)②c(CH3COO-)+c(CH3COOH)=2c(Na+)=0.1mol?L-1
③c(CH3COOH)=0.05-10-4+10-10mol?L-1(各2分)
略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

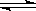 CH3COO-+ H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变大的是( )
CH3COO-+ H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变大的是( )