题目内容
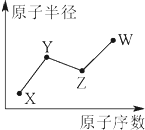
【题目】主族元素W、X、Y、Z的原子序数依次增大,W的原子最外层电子数是次外层电子数的3倍。X、Y和Z分属不同的周期,它们的原子序数之和是W原子序数的5倍。在由元素W、X、Y、Z组成的所有可能的二组分化合物中,由元素W与Y形成的化合物M的熔点最高。请回答下列问题:
(1)W元素原子的L层电子排布式为___________ ,W3分子的空间结构为___________;
(2)X单质与水发生主要反应的方程为___________;
(3)化合物M的化学式为___________,其晶体结构与NaCl相同,而熔点高于NaCl.M熔点较高的原因是___________,将一定量的化合物ZX负载在M上可制得ZX/M催化剂,用于催化碳酸二甲酯与月桂醇酯交换合成碳酸二月桂酯.在碳酸二甲酯分子中,碳原子采用的杂化方式有___________ ,O-C-O的键角约为___________;
(4)X、Y、Z可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角,Z处于体心位置,则该晶体的组成X:Y:Z= ___________;
(5)许多金属盐都可以发生焰色反应,其原因是___________。
【答案】(1)2s22p4;V型;
(2)2F2+2H2O═4HF+O2;
(3)MgO;MgO的晶格能大于NaCl的晶格能;sp2和sp3;120°;
(4)3:1:1.
(5)灼烧时电子从基态到激发态,当从激发态回到基态时放出能量以光的形式放出,从而出现不同的颜色
【解析】试题分析:主族元素W、X、Y、Z的原子序数依次增大,W的原子最外层电子数是次外层电子数的3倍,则W有3个电子层,最外层电子数为6,故W为氧元素;X,Y,Z分属不同的周期,且主族元素W、X、Y、Z的原子序数依次增大.X不可能为第三周期元素,若为第三周期,X、Y、Z的原子序数之和大于W原子序数的5倍,所以可以断定X也在第二周期,且原子序数比氧元素大,故X为F元素;故Y、Z的原子序数之和为8×5-9=31,平均原子序数为15.5,故Y处于第三周期,Z处于第四周期,Z的原子序数大于18,若Y为Na元素,则Z为Ca元素,若Y为Mg元素,则Z为K元素,X的原子序数再增大,不符合题意,由于元素W与Y形成的化合物M的熔点最高,故Y为Mg元素,Z为K元素.
(1)W为氧元素,O原子的L层电子排布式为2s22p4;O3分子中中心氧原子价层电子对数=2+![]() ×(62×2)=3、含有1对孤电子对,故O3空间构型为V型,故答案为:2s22p4;V型;
×(62×2)=3、含有1对孤电子对,故O3空间构型为V型,故答案为:2s22p4;V型;
(2)X为F元素,对应的单质具有强氧化性,可与水反应生成HF和氧气,反应的方程式为:2F2+2H2O═4HF+O2,故答案为:2F2+2H2O═4HF+O2;
(3)由上述分析可知,M为MgO,其晶体结构与NaCl相同,而熔点高于NaCl,由于MgO晶体中离子的电荷多,晶格能大,故MgO熔点较高;在碳酸二甲酯分子中-OCH3,C原子4个单键,采取sp3杂化,在酯基![]() 中,C原子呈2个C-O单键,属于σ键,1个C=O双键,双键按单键计算,故中心C原子的杂化轨道数为3,采取sp2杂化,为平面正三角形,键角为120°,故O-C-O的键角约为120°,故答案为:MgO;MgO的晶格能大于NaCl的晶格能;sp2和sp3;120°;
中,C原子呈2个C-O单键,属于σ键,1个C=O双键,双键按单键计算,故中心C原子的杂化轨道数为3,采取sp2杂化,为平面正三角形,键角为120°,故O-C-O的键角约为120°,故答案为:MgO;MgO的晶格能大于NaCl的晶格能;sp2和sp3;120°;
(4)F、Mg、K形成立方晶体结构的化合物,晶胞中F占据所有棱的中心,晶胞中F原子数目为12×![]() =3,Mg位于顶角,晶胞中Mg原子数目为8×
=3,Mg位于顶角,晶胞中Mg原子数目为8×![]() =1,K处于体心位置,晶胞中含有1个K原子,则该晶体的组成为F:Mg:K=3:1:1,故答案为:3:1:1;
=1,K处于体心位置,晶胞中含有1个K原子,则该晶体的组成为F:Mg:K=3:1:1,故答案为:3:1:1;
(5)含有元素K的盐的焰色反应为紫色,许多金属盐都可以发生焰色反应,其原因为:灼烧时电子从基态到激发态,当从激发态回到基态时放出能量以光的形式放出,从而出现不同的颜色,故答案为:灼烧时电子从基态到激发态,当从激发态回到基态时放出能量以光的形式放出,从而出现不同的颜色。

 发散思维新课堂系列答案
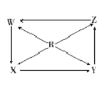
发散思维新课堂系列答案【题目】如图R、W、X、Y、Z为五种物质,若箭头表示能进一步转化的常见反应,则其中常温下能实现图示转化关系的是( )
选项 | R | W | X | Y | Z |
|
A | Si | SiO2 | H2SiO3 | NaSiO3 | SiCl4 | |
B | Na | Na2O | Na2O2 | Na2CO3 | NaOH | |
C | Fe | Fe(OH)2 | FeCl2 | FeCl3 | Fe(NO3)3 | |
D | Al | NaAlO2 | Al2(SO4)3 | AlCl3 | Al(NO3)3 |