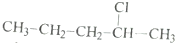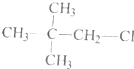题目内容
15.下列说法正确的是( )| A. | 离子化合物中可能含有共价键 | B. | 分子晶体中的分子内不含有共价键 | ||
| C. | 分子晶体中一定有非极性共价键 | D. | 分子晶体中分子一定紧密堆积 |
分析 A.共价键可存在于单质、化合物中;
B.稀有气体分子晶体中不存在化学键;
C.分子晶体中可能不存在化学键;
D.冰中水分子间存在氢键,不具有分子密堆积特征.
解答 解:A.离子化合物中可能含有共价键,如离子化合物KOH中含O-H共价键,可能不含共价键如NaCl,故A正确;
B.多原子分子内含共价键如HCl,稀有气体分子晶体中不含化学键,故B错误;
C.稀有气体分子晶体中不含化学键,故C错误;
D.冰中水分子间存在氢键,氢键具有方向性,所以分子晶体冰不具有分子密堆积特征,故D错误;
故选A.
点评 本题考查化学键,为高频考点,把握化学键的形成及物质中的化学键为解答的关键,注意稀有气体中不含化学键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
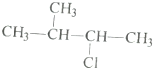
5.下列烷烃的命名错误的是( )
| A. | 3-甲基丁烷 | B. | 2-甲基-3-乙基戊烷 | ||
| C. | 2,2-二甲基丁烷 | D. | 2,3-二甲基丁烷 |
6.将1 mol冰醋酸加人到一定量的蒸馏水中最终得到1L溶液.下列各项中,表明已达到电离平衡状态的是( )
| A. | 醋酸的浓度达到1 mol•L-1 | |
| B. | H+的浓度达到0.5 mol•L-1 | |
| C. | 醋酸分子的浓度、醋酸根离子的浓度、H+的浓度均为0.5 mol•L-1 | |
| D. | 醋酸分子电离成离子的速率和离子重新结合成醋酸分子的速率相等. |
3.湿化学法(NPP-法)制备纳米级活性氧化锌,可以用氧化锌粗品(含有FeO、Fe2O3、CuO杂质)为原料,采用酸浸出锌,经过多次净化除去原料中的杂质,然后沉淀获得碱式碳酸锌,最后焙烧获得活性氧化锌.其化学工艺流程如图:
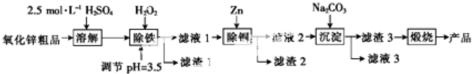
已知:溶液中Fe2+、Fe3+、Cu2+、Zn2+以氢氧化物的形式沉淀时的pH如表:
(1)实验室用98%浓H2SO4(ρ=1.84g/cm3)来配制100ml 2.5mol/L稀H2SO4所需的玻璃仪器有烧杯、胶头滴管、00mL容量瓶、量筒、玻璃棒.
(2)上述流程图中pH=12的Na2CO3溶液中阴离子的浓度由大到小的顺序为c(CO32-)>c(OH-)>c(HCO3-).
(3)滤渣1是Fe(OH)3(填化学式,下同),滤渣2是Cu、Zn.加入H2O2时发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)“沉淀”得到ZnCO3•2Zn(OH)2•H2O,“煅烧”在450~500℃下进行,“煅烧”反应的化学方程式为ZnCO3•2Zn(OH)2•H2O$\frac{\underline{\;450℃-500℃\;}}{\;}$3ZnO+CO2↑+3H2O↑.

已知:溶液中Fe2+、Fe3+、Cu2+、Zn2+以氢氧化物的形式沉淀时的pH如表:
| 离子 | 开始沉 淀的pH | 完全沉 淀的pH |
| Fe2+ | 6.4 | 8.4 |
| Fe3+ | 2.7 | 3.2 |
| Cu2+ | 5.2 | 6.7 |
| Zn2+ | 6.8 | 9.0 |
(2)上述流程图中pH=12的Na2CO3溶液中阴离子的浓度由大到小的顺序为c(CO32-)>c(OH-)>c(HCO3-).
(3)滤渣1是Fe(OH)3(填化学式,下同),滤渣2是Cu、Zn.加入H2O2时发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)“沉淀”得到ZnCO3•2Zn(OH)2•H2O,“煅烧”在450~500℃下进行,“煅烧”反应的化学方程式为ZnCO3•2Zn(OH)2•H2O$\frac{\underline{\;450℃-500℃\;}}{\;}$3ZnO+CO2↑+3H2O↑.
7.下列各组元素中,按从左到右的顺序,原子序数递增、元素的最高正化合价也递增的是( )
| A. | Na,Mg,Al,Si | B. | Na,Be,B,C | C. | P,S,Cl,Ar | D. | C,N,O,F |
4.下列热化学方程式书写正确的是(△H的绝对值均正确)( )
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1367.0 kJ/mol(燃烧热) | |
| B. | S(s)+O2(g)═SO2(g)△H=-269.8kJ/mol(反应热) | |
| C. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热) | |
| D. | 2NO2═O2+2NO△H=+116.2kJ/mol(反应热) |
5.下列四个选项是在不同的情况下对化学反应A(g)+3B(g)?2C(g)+2D(g) 测得用不同物质表示的反应速率,其中表示该化学反应的反应速率最快的是( )
| A. | v(D)=0.6 mol•L-1•min-1 | B. | v(B)=0.45 mol•L-1•s-1 | ||
| C. | v(C)=0.40 mol•L-1•min-1 | D. | v(A)=0.2 mol•L-1•s-1 |