题目内容
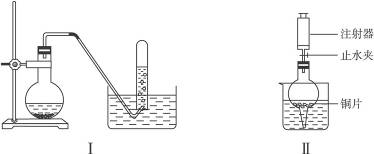
某研究性学习小组为完成浓硝酸、稀硝酸、NO2、NO的部分实验,并有效地防止NO2、NO的污染。设计了如下图所示的装置进行实验。
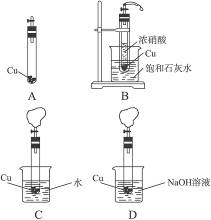
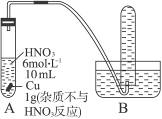
先将适量块状CaCO3和过量铜片放入底部开一小孔的试管中,塞上塞子(连有带活塞的导气管),如图A所示,再将试管放入盛有适量盐酸的烧杯中,打开活塞,发生反应:CaCO3+2HCl====CaCl2+H2O+CO2↑,用产生的CO2排尽试管内的空气。
(1)待CaCO3反应完全后,关闭活塞,在导气管上套一排尽空气的气球,然后将试管放入盛有浓硝酸的大试管中,如图B所示。再打开活塞,观察到的现象是_________________。上述现象说明____________________________________________________。有关反应的离子方程式为_____________________________________________________________________。
(2)上述反应进行一段时间后,关闭活塞,迅速将带小孔的试管取出,放入盛有适量水的烧杯中,如图C所示,再打开活塞,观察到的现象是_______________________________。
(3)关闭活塞,迅速将试管取出,放入盛有足量NaOH溶液的烧杯中,如图D所示。打开活塞,NO、NO2与NaOH溶液发生反应:2NaOH+NO+NO2====2NaNO2+H2O,气球逐渐变小,试管内液面上升。NO不能单独与NaOH溶液反应,若要将氮的氧化物完全吸收,应该如何操作?___________________________________________________。

先将适量块状CaCO3和过量铜片放入底部开一小孔的试管中,塞上塞子(连有带活塞的导气管),如图A所示,再将试管放入盛有适量盐酸的烧杯中,打开活塞,发生反应:CaCO3+2HCl====CaCl2+H2O+CO2↑,用产生的CO2排尽试管内的空气。
(1)待CaCO3反应完全后,关闭活塞,在导气管上套一排尽空气的气球,然后将试管放入盛有浓硝酸的大试管中,如图B所示。再打开活塞,观察到的现象是_________________。上述现象说明____________________________________________________。有关反应的离子方程式为_____________________________________________________________________。
(2)上述反应进行一段时间后,关闭活塞,迅速将带小孔的试管取出,放入盛有适量水的烧杯中,如图C所示,再打开活塞,观察到的现象是_______________________________。
(3)关闭活塞,迅速将试管取出,放入盛有足量NaOH溶液的烧杯中,如图D所示。打开活塞,NO、NO2与NaOH溶液发生反应:2NaOH+NO+NO2====2NaNO2+H2O,气球逐渐变小,试管内液面上升。NO不能单独与NaOH溶液反应,若要将氮的氧化物完全吸收,应该如何操作?___________________________________________________。
(1)铜片逐渐溶解,产生红棕色气体,气球逐渐膨胀,大试管中液体变为蓝色,烧杯内析出固体 铜与浓硝酸反应生成NO2气体和Cu(NO3)2蓝色溶液,该反应为放热反应 Cu+4H++2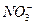 ====Cu2++2NO2↑+2H2O
====Cu2++2NO2↑+2H2O
(2)先看到气球逐渐变小,气体颜色逐渐变淡,烧杯内溶液变为浅蓝色,后气球慢慢膨胀
(3)取下气球,打开活塞(待试管内液面降到与烧杯中液面相平时),关闭活塞(此时试管内液面上升,气体颜色逐渐变淡)。重复上述操作至打开活塞不再出现红棕色为止
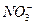 ====Cu2++2NO2↑+2H2O
====Cu2++2NO2↑+2H2O(2)先看到气球逐渐变小,气体颜色逐渐变淡,烧杯内溶液变为浅蓝色,后气球慢慢膨胀
(3)取下气球,打开活塞(待试管内液面降到与烧杯中液面相平时),关闭活塞(此时试管内液面上升,气体颜色逐渐变淡)。重复上述操作至打开活塞不再出现红棕色为止
根据题意弄清各仪器、试剂的作用是解题的关键。装置A相当于一个简易启普发生器,用CO2排尽试管内的空气的目的是避免NO被空气氧化成NO2而产生干扰;装置B中烧杯中饱和石灰水与反应无关,但可利用Ca(OH)2的溶解性的特殊性来检验反应是否放热;装置C中水可与气球内NO2反应3NO2+H2O====2HNO3+NO,HNO3再与Cu反应8HNO3+3Cu====3Cu(NO3)2+2NO↑+4H2O,因此气球先变小后回胀;装置D中NaOH可吸收NO2、NO混合气体,但不单独与NO反应,必须使NO与空气接触氧化成NO2再吸收。

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
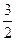 O2(g) ΔH=+765.2kJ·mol-1
O2(g) ΔH=+765.2kJ·mol-1 2NH3(g)。设在容积为2.0L的密闭容器中充入0.60mol N2(g)和1.60 mol H2(g),.反应在一定条件下达到平衡时,NH3的物质的量分数(NH2的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0L的密闭容器中充入0.60mol N2(g)和1.60 mol H2(g),.反应在一定条件下达到平衡时,NH3的物质的量分数(NH2的物质的量与反应体系中总的物质的量之比)为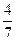 。计算
。计算