题目内容
下列实验操作、实验现象及解释与结论都正确的是( )
| 选项 | 实验操作 | 实验现象 | 解释与结论 |
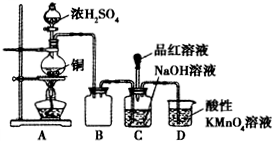
| A | 将乙醇与浓硫酸共热至170℃所得气体通入酸性KMnO4溶液中 | KMnO4溶液褪色 | 乙醇发生消去反应,气体中含只有乙烯 |
| B | 淀粉溶液和稀H2SO4混合加热,然后加新制的Cu(OH)2悬浊液加热至沸腾 | 有红色沉淀产生 | 淀粉水解了,且产物有还原性 |
| C | 向甲苯中滴入少量浓溴水,振荡,静置 | 溶液分层,上层呈橙红色,下层几乎无色 | 甲苯和溴发生取代反应,使溴水褪色 |
| D | 向蔗糖中加入浓硫酸 | 变黑,放热,体积膨胀,放出刺激性气体 | 浓硫酸具有脱水性和强氧化性,反应中生成C、SO2和CO2等 |
| A.A | B.B | C.C | D.D |
A、乙醇的消去反应中,碳和浓硫酸之间会反应生成具有还原性的二氧化硫气体,该气体能使高锰酸钾褪色,故A错误;
B、淀粉溶液和稀H2SO4混合加热,水解产物是葡萄糖,它和新制的Cu(OH)2悬浊液的反应必须在碱性环境下发生,故B错误;
C、甲苯和溴水之间不会发生取代反应,只有在铁催化下,才鞥和纯液溴反应,故C错误;
D、浓硫酸具有脱水性和强氧化性,向蔗糖中加入浓硫酸变黑,放热,体积膨胀,碳和浓硫酸之间反应放出刺激性气体SO2,还会产生二氧化碳等气体,故D正确.
故选D.
B、淀粉溶液和稀H2SO4混合加热,水解产物是葡萄糖,它和新制的Cu(OH)2悬浊液的反应必须在碱性环境下发生,故B错误;
C、甲苯和溴水之间不会发生取代反应,只有在铁催化下,才鞥和纯液溴反应,故C错误;
D、浓硫酸具有脱水性和强氧化性,向蔗糖中加入浓硫酸变黑,放热,体积膨胀,碳和浓硫酸之间反应放出刺激性气体SO2,还会产生二氧化碳等气体,故D正确.
故选D.

练习册系列答案
相关题目