题目内容
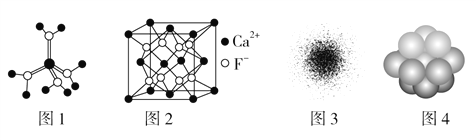
【题目】如果1mol金刚石的质量为a g,密度为ρg·cm﹣3,请计算出每个碳原子的共价半径________(两个原子核之间距离的一半)(设碳原子为紧密堆积结构,见图)。(用含a,ρ,NA的式子表示。NA表示阿伏加德罗常数的值)

【答案】![]()
【解析】由金刚石的晶胞结构可知,晶胞内部有4个C原子,面心上有6个C原子,顶点有8个C原子,所以金刚石晶胞中C原子数目为4+6×1/2+8×1/8=8;若C原子半径为r,金刚石晶胞的边长为L,,根据硬球接触模型,则正方体对角线长度的1/4就是C—C键的键长,即![]() L=2r,L=8/
L=2r,L=8/ ![]() ,晶胞的体积为L3= [8/
,晶胞的体积为L3= [8/ ![]() ]3cm3;因此8a/ρNA=[8/
]3cm3;因此8a/ρNA=[8/ ![]() ]3,解之得到r=
]3,解之得到r=![]() cm;正确答案:
cm;正确答案:![]() 。
。

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目