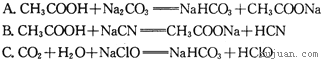题目内容
【题目】云阳龙缸云端廊桥曾被詟为“世界第一悬挑玻璃景观廊桥”,所用钢化玻璃因其优良的性能广泛应用于日常生活,但由于制作玻璃时里面含有极少量硫化镍,使得钢化玻璃在极限条件下的使用受到限制.
(1)基态硫原子价层电子的轨道表达式(电子排布图)为____________,基态镍原子中核外电子占据最高能层的符号为_____________.
(2)Ni(CO)4常用于制备纯镍,溶于乙醇、CCl4、苯等有机溶剂,为___________晶体,Ni(CO)4空间构型与甲烷相同,中心原子的杂化轨道类型为___________,写出与配体互为等电子体的阴离子__________________________________________________________(任写一种).
(3)与硫同族的硒元素有两种常见的二元含氧酸,请比较它们酸性强弱 > (填化学式)______,理由是_______________________________________________________________.
(4)H2S的键角__________(填“大于”“小于””等于”)H2O的键角,请从电负性的角度说明理由___________________________________________________.
(5)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的空隙中,已知Ni2+半径为69nm,O2-半径为140nm,阿伏伽德罗常数为NA,NiO晶体的密度为_________g/cm3(只列出计算式).

【答案】![]() N分子晶体sp3杂化CN- 或C22-H2SeO4>H2SeO3(1分),因为H2SeO4中非羟基氧数目比H2SeO3多,导致H2SeO4中Se元素的正电性更高,对羟基中共用电子对的吸引能力更强,使得羟基氢更易电离小于氧元素的电负性比硫元素更强,对键合电子的吸引力更强,键合电子之间的排斥力更大,所以键角更大正八面体
N分子晶体sp3杂化CN- 或C22-H2SeO4>H2SeO3(1分),因为H2SeO4中非羟基氧数目比H2SeO3多,导致H2SeO4中Se元素的正电性更高,对羟基中共用电子对的吸引能力更强,使得羟基氢更易电离小于氧元素的电负性比硫元素更强,对键合电子的吸引力更强,键合电子之间的排斥力更大,所以键角更大正八面体![]() 或
或![]()
【解析】
(1)S位于周期表中第3周期第ⅥA族,基态硫原子的价电子排布式为3s23p4,则基态硫原子价层电子的轨道表达式(电子排布图)为:![]() ,Ni位于周期表中第4周期第ⅤⅢ族,基态Ni核外电子占据最高能层为N,故答案为:
,Ni位于周期表中第4周期第ⅤⅢ族,基态Ni核外电子占据最高能层为N,故答案为:![]() ;N;
;N;
(2)根据相似相溶原理判断,Ni(CO)4溶于乙醇、CCl4、苯等有机溶剂,所以可判断Ni(CO)4为分子晶体,Ni(CO)4空间构型与甲烷相同,甲烷为正四面体,中心C原子为sp3杂化,所以可判断中心原子的杂化轨道类型为sp3,等电子体是指原子总数相同,价电子总数相同的微粒,Ni(CO)4的配位为CO,O可用N-或者C2-代替,所以形成的等电子体可以为:CN-或C22-,故答案为:分子晶体;sp3;CN-或C22-;
(3)与硫同族的硒元素有两种常见的二元含氧酸,分别为H2SeO4和H2SeO3,酸性强弱H2SeO4>H2SeO3,理由为:因为H2SeO4中非羟基氧数目比H2SeO3多,导致H2SeO4中Se元素的正电性更高,对羟基中共用电子对的吸引能力更强,使得羟基氢更易电离,故答案为:H2SeO4>H2SeO3;因为H2SeO4中非羟基氧数目比H2SeO3多,导致H2SeO4中Se元素的正电性更高,对羟基中共用电子对的吸引能力更强,使得羟基氢更易电离;
(4)根据价层电子对互斥理论,孤电子对存在可使键角变小,电负性O大于S,对键合电子的吸引力更强,键合电子之间的排斥力更大,所以键角更大,故答案为:小于;氧元素的电负性比硫元素更强,对键合电子的吸引力更强,键合电子之间的排斥力更大,所以键角更大;
(5)根据晶胞结构分析,阴离子采取面心立方堆积,形成八面体空隙和四面体空隙,但Ni2+填充在八面体空隙,由于阴离子是面心立方堆积,所以晶胞边长为a=2r(Ni2+)+2r(O2-)=418nm,不妨取1mol这样的晶胞,即有NA个这样的晶胞,则晶体密度为ρ=![]() =
=![]() g/cm3,故答案为:正八面体;
g/cm3,故答案为:正八面体;![]() 。
。

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案