题目内容
自然界各种原生铜的硫化物经氧化、淋滤后变成CuSO4溶液,并向深部渗透时,遇到闪锌矿(ZnS)和方铅矿(PbS),便慢慢地转变为铜蓝(CuS),下列有关该过程的解释及说法不合理的是
A.原生铜的硫化物具有还原性
B.常温时ZnS、PbS、CuS都难溶于水,CuSO4可溶于水
C.铜蓝的形成过程是:ZnS(s)+Cu2+ CuS(s)+Zn2+
CuS(s)+Zn2+
D.硝酸型酸雨不利于铜蓝的形成:CuS+2H+=Cu2++H2S↑
练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
卤族元素的单质能与H2反应
H2+F2=2HF | 在暗处能剧烈化合并发生爆炸 |
H2+Cl2=2HCl | 光照或点燃发生反应 |
H2+Br2=2HBr | 加热至一定温度才能反应 |
H2+I2=2HI | 不断加热才能缓慢反应,生成的HI会分解 |
(1)卤族元素位于周期表中的______________族。
(2)用电子式表示HCl的形成过程______________。
(3)依据上表,可以推测出:随着原子序数的递增,___________(填字母)。
a. 单质的熔沸点逐渐升高 b. 元素的非金属性逐渐减弱
c. 卤化氢的还原性依次减弱 d. 卤化氢的稳定性依次减弱
(4)不同卤素原子之间可形成卤素互化物,其性质与卤素单质相近。写出BrCl和SO2在水溶液中发生反应的化学方程式___________。


 关系式正确的是( )
关系式正确的是( )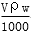 B.c=
B.c=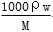 C.w%=
C.w%= % D.c=
% D.c=
 H2CO3+2OH—
H2CO3+2OH—
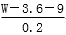 B.
B. 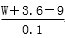
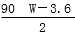 D.
D.