题目内容
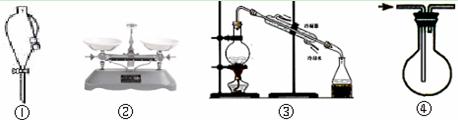
某化学小组模拟工业生产制取HNO3,设计下图所示装置,其中a为一个可持续鼓入空气的橡皮球。
请回答下列问题:
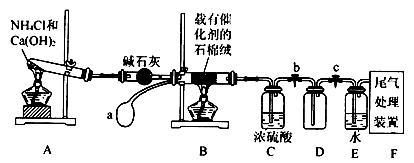
(1)写出装置A中主要反应的化学方程式 。
(2)实验结束后,关闭止水夹b、c,将装置D,浸入冰水中,现象是
(3)装置C中浓H2SO4的作用是 。
(4)请你帮助该化学小组设计实验室制取NH3的另一方案
(5)干燥管中的碱石灰用于干燥NH3,某同学思考是否可用无水氯化钙代替碱石灰,并设计右图所示装置(仪器固定装置省略未画)进行验证。实验步骤如下:
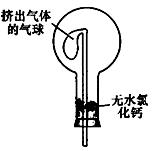
①用烧瓶收集满干燥的氨气,立即塞上如图所示的橡胶塞。
②正立烧瓶,使无水氯化钙固体滑入烧瓶底部,摇动,可以观察到的现象是 ,由此,该同学得出结论:不能用CaCl2代替碱石灰。
请回答下列问题:

(1)写出装置A中主要反应的化学方程式 。
(2)实验结束后,关闭止水夹b、c,将装置D,浸入冰水中,现象是
(3)装置C中浓H2SO4的作用是 。
(4)请你帮助该化学小组设计实验室制取NH3的另一方案
(5)干燥管中的碱石灰用于干燥NH3,某同学思考是否可用无水氯化钙代替碱石灰,并设计右图所示装置(仪器固定装置省略未画)进行验证。实验步骤如下:

①用烧瓶收集满干燥的氨气,立即塞上如图所示的橡胶塞。
②正立烧瓶,使无水氯化钙固体滑入烧瓶底部,摇动,可以观察到的现象是 ,由此,该同学得出结论:不能用CaCl2代替碱石灰。
(1)Ca(OH)2+2NH4Cl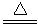 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
(2)气体颜色变浅 (3)吸收未反应的NH3和水蒸气
(4)加热浓氨水(或浓氨水中加固体碱性物质或加CaO或NaOH固体或加碱石灰等)
(5)气球膨胀(或气球变大,鼓起等)
 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O(2)气体颜色变浅 (3)吸收未反应的NH3和水蒸气
(4)加热浓氨水(或浓氨水中加固体碱性物质或加CaO或NaOH固体或加碱石灰等)
(5)气球膨胀(或气球变大,鼓起等)
略

练习册系列答案
相关题目
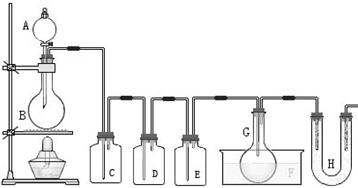
 ,则F中盛有 ,作用是______________________。
,则F中盛有 ,作用是______________________。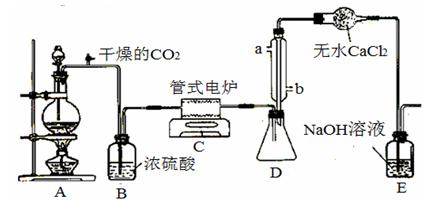
 、CO32-、OH
、CO32-、OH 。请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑盐类的水解).
。请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑盐类的水解). L-1 H2SO4 b.0.01mol
L-1 H2SO4 b.0.01mol 预期现象和结论
预期现象和结论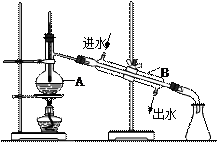
 ,B仪器的名称是 。
,B仪器的名称是 。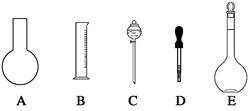
 度线,则所得溶液浓度 0.8 mol/L(填“大于”、“等于”或“小于”,下同)。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度 0.8 mol/L。
度线,则所得溶液浓度 0.8 mol/L(填“大于”、“等于”或“小于”,下同)。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度 0.8 mol/L。