题目内容
【题目】化合物Z具有广谱抗菌活性,可利用X和Y反应获得。下列有关说法正确的是( )
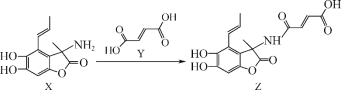
A.有机物X的分子式为C12H13O4N
B.有机物Y可以和乙醇发生缩聚反应
C.有机物Y中所有原子可能在同一平面上
D.1mol有机物Z与足量NaOH溶液反应最多消耗4mol NaOH
【答案】AC
【解析】
A.有机物结构中的每个节点为碳原子,每个碳原子形成4个共价键,不足键由氢原子补齐,则有机物X的分子式为C12H13O4N,故A正确;
B.有机物Y中含有羧基,可以和乙醇发生酯化反应,故B错误;
C.有机物Y中含有碳碳双键和碳氧双键,双键属于平面结构,与双键上的原子直接相连的所有原子可能在同一平面上,故C正确;
D.有机物Z中,酚羟基、酯基、羧基均可与氢氧化钠反应,1mol有机物Z中含有2mol酚羟基、1mol羧基、1mol酯基,1mol酯基水解后又可形成1mol酚羟基和1mol羧基,则与足量NaOH溶液反应最多消耗5mol NaOH,故D错误;
答案选AC。

练习册系列答案
相关题目