题目内容
含CN- 的废水有剧毒,可用液氯在碱性条件下将其氧化成OCN-,OCN- 再进一步被氧化为无毒物质。有关反应如下:
⑴ KCN+2KOH+Cl2 → KOCN+2KCl+H2O 被氧化的元素是 。
⑵ 写出KOCN在KOH溶液中与氯气反应生成无毒物质的化学方程式:
。
⑶ 某厂废水中含KCN,其浓度为650mg / L,该废水的密度为1 g/mL。现用氯氧化法处理,该厂每日处理上述废水20t,使KCN完全转化为无毒物质,每天至少需液氯 kg(保留到小数点后1位)。
⑴ KCN+2KOH+Cl2 → KOCN+2KCl+H2O 被氧化的元素是 。
⑵ 写出KOCN在KOH溶液中与氯气反应生成无毒物质的化学方程式:
。
⑶ 某厂废水中含KCN,其浓度为650mg / L,该废水的密度为1 g/mL。现用氯氧化法处理,该厂每日处理上述废水20t,使KCN完全转化为无毒物质,每天至少需液氯 kg(保留到小数点后1位)。
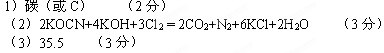
⑴由KCN → KOCN碳元素化合价升高,被氧化的元素是碳;
⑵2KOCN+4KOH+3Cl2=2CO2+N2+6KCl+2H2O,N由-3价变成0价,共变6价;
⑶20t废水的体积为:20×106g/1 g/mL=20×106mL, 即20×103L,含KCN为20×103L×650mg / L=1300×103 mg,即:13kg, 再由KCN+2KOH+Cl2 → KOCN+2KCl+H2O和2KOCN+4KOH+3Cl2=2CO2+N2+6KCl+2H2O,得
关系式:2KCN ~ 5Cl2
130 355
13kg m
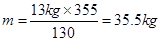

练习册系列答案
相关题目
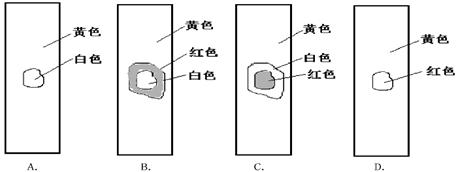
 试纸中部,观察到的现象是
试纸中部,观察到的现象是