题目内容
(12分).可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)请填空:
(1)试管a中需要加入浓硫酸、冰醋酸和乙醇各2mL,正确加入顺序操作是_____________________________________________。
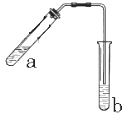
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是 ____________
(3)实验中加热试管的目的是:① ________________________________
②__________________________________________________________________
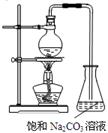
(4)试管b中加有饱和Na2CO3溶液 ,其作用是_____________________________
(5)反应结束后,振荡试管b静置,观察到的现象是___________________________
(6)制取乙酸乙酯的化学方程式___________________________
(1)试管a中需要加入浓硫酸、冰醋酸和乙醇各2mL,正确加入顺序操作是_____________________________________________。

(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是 ____________
(3)实验中加热试管的目的是:① ________________________________
②__________________________________________________________________
(4)试管b中加有饱和Na2CO3溶液 ,其作用是_____________________________
(5)反应结束后,振荡试管b静置,观察到的现象是___________________________
(6)制取乙酸乙酯的化学方程式___________________________
(12分)(1)先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,再加冰醋酸 (2分)
(2)在试管a中加入几粒沸石(或碎瓷片) (2分)
(3) ①加快反应速率(1分)
②及时将产物乙酸乙酯蒸出,以利于平衡向生成乙酸乙酯的方向移动 (1分)
(4)吸收随乙酸乙酯蒸出的少量酸性物质和乙醇(2分)
(5)b中的液体分层,上层是透明的油状液体 (2分)
(6)方程式: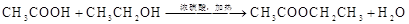 (2分)
(2分)
(2)在试管a中加入几粒沸石(或碎瓷片) (2分)
(3) ①加快反应速率(1分)
②及时将产物乙酸乙酯蒸出,以利于平衡向生成乙酸乙酯的方向移动 (1分)
(4)吸收随乙酸乙酯蒸出的少量酸性物质和乙醇(2分)
(5)b中的液体分层,上层是透明的油状液体 (2分)
(6)方程式:
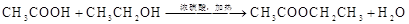 (2分)
(2分)试题分析:(1)制取乙酸乙酯一般用浓硫酸、乙醇和乙酸混合制取,在混合溶液时要注意顺序,因为浓硫酸的密度比乙醇和乙酸大,防止液体放热剧烈飞溅,最正确顺序应该是先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,再加冰醋酸;
(2)直接加热纯液体会发生暴沸现象,防暴沸一般在试管中加入几粒沸石(或碎瓷片);
(3)加热试管的目的主要有 ①温度升高,加快反应速率,②因为该反应是可逆反应,为了提高产率,及时将产物乙酸乙酯蒸出,以利于平衡向生成乙酸乙酯的方向移动;
(4)蒸馏乙酸乙酯的同时也会蒸馏出易挥发的乙醇和乙酸,饱和Na2CO3溶液有几个作用:吸收随乙酸乙酯蒸出的少量酸性物质和乙醇,便于乙酸乙酯的分层;
(5)乙酸乙酯不溶于饱和碳酸钠,在上层是透明的油状液体;
(6)根据酯化反应原理,羧酸脱羟基,醇脱去氢原子,可以写出方程式:

点评:属于简单题。

练习册系列答案
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
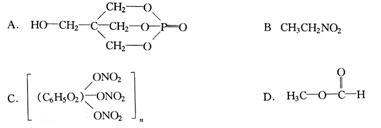
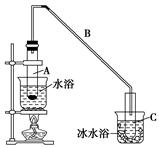
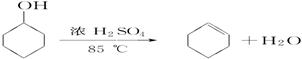
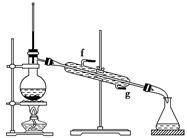
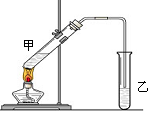
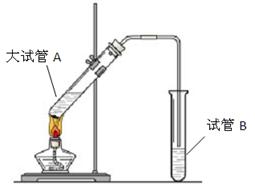
 转化关系中,B能使溴的四氯化碳溶液褪色。
转化关系中,B能使溴的四氯化碳溶液褪色。