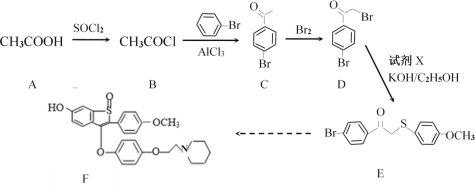
题目内容
【题目】常温下,用0.1mol/LKOH溶液滴定10mL0.1mol/LHA溶液的滴定曲线如图所示。下列说法不正确的是( )
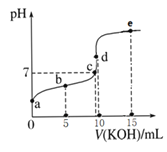
A.a点pH约为3,可以判断HA是弱酸
B.b点溶液:c(A-)>c(K+)>c(HA)>c(H+)>c(OH-)
C.c点溶液:c(K+)=c(A-)
D.水的电离程度:c点>d点
【答案】D
【解析】
A.a点为0.1mol/LHA溶液,若是强酸,pH=1,但pH约为3,HA是弱酸,A正确;
B.b点溶液中溶质为等物质的量的KA和HA,溶液显酸性,离子浓度关系为:c(A-)>c(K+)>c(HA)>c(H+)>c(OH-),B正确;
C.c点溶液的pH=7,c(H+)=c(OH-),根据电荷守恒,c(K+)=c(A-),C正确;
D.c点溶液的pH=7,溶质为HA和KA,HA抑制水的电离,d点溶液的溶质为KA,KA促进水的电离,水的电离程度:c点<d点,D错误;故答案为:D。

【题目】下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题:
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(1)原子半径最小的元素是____(填元素名称),写出⑧的原子结构示意图______。
(2)最高价氧化物对应的水化物中,碱性最强的是___(用化学式回答,下同),酸性最强的是___。
(3)①与⑤形成的化合物中,化学键类型为_____。
(4)⑦与⑨形成的化合物的电子式为___,②与④形成的原子个数比为1:2的化合物的结构式为____。
(5)③、④、⑥的原子半径由大到小的顺序为_____(用元素符号回答)。
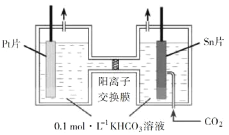
(6)为探究元素②和⑧的非金属性强弱,某同学设计了如图所示的装置进行实验(夹持仪器已略去,装置气密性良好)。请回答:
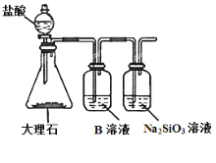
a.溶液B的作用是_______
b.若看到____现象,即可证明酸性_______(用化学式回答),则非金属性_______(用元素符号回答)。
c.上述实验中,能说明②和⑧非金属性强弱的化学方程式是_____________。