题目内容
工业生产的纯碱中常含有少量的NaCl杂质.某校研究性学习活动小组为了测定混合物中纯碱的质量分数,拟使用下图实验装置,先测定一定量的样品和酸反应放出二氧化碳的质量,再计算混合物中纯碱的质量分数.
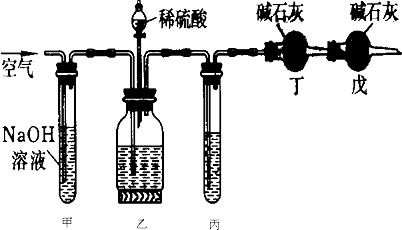
(1)装稀硫酸的装置名称 .
(2)甲装置的作用是 ;戊装置的作用是 .
(3)乙装置反应前先通数分钟空气的作用是 ,甲装置反应的离子方程式是 .
(4)丙装置中试剂是 若去掉丙装置,测得纯碱的质量分数会 (填“偏大”或“偏小”).
(5)若取ng样品装入广口瓶,且反应前填满碱石灰的干燥管丁总质量为mg,实验结束后称得干燥管丁的总质量为w,则Na2CO3质量分数的计算式为 .

(1)装稀硫酸的装置名称
(2)甲装置的作用是
(3)乙装置反应前先通数分钟空气的作用是
(4)丙装置中试剂是
(5)若取ng样品装入广口瓶,且反应前填满碱石灰的干燥管丁总质量为mg,实验结束后称得干燥管丁的总质量为w,则Na2CO3质量分数的计算式为
分析:(1)装稀硫酸的装置是分液漏斗;
(2)实验装置中会残留部分二氧化碳,影响丁中二氧化碳质量的测定,需要通入空气将装置内的二氧化碳完全排入丁中被吸收,空气中含有二氧化碳,故应先用氢氧化钠溶液吸收,防止影响二氧化碳的测定;
空气中二氧化碳、水蒸气进入丁中影响二氧化碳的质量测定,导致测定二氧化碳的质量增大,戊装置的作用是吸收二氧化碳中的水蒸气,防止进入装置丁中;
(3)装置中含有二氧化碳,不将二氧化碳排尽,会使测定的二氧化碳的质量增大,故反应前应先通空气,排尽装置内的二氧化碳;
装置甲中二氧化碳与氢氧化钠反应生成碳酸钠与水;
(4)从装置乙中产生导出的气体中含有水,如果不除去气体中的水,会使丁中测定的二氧化碳的质量增大,故加入装置丁的二氧化碳应干燥,故装置丙中盛放的试剂是浓硫酸;
(5)由题意可知,反应生成的二氧化碳的质量为(w-m)g,计算二氧化碳的物质的量,根据碳元素守恒二氧化碳的物质的量等于样品中碳酸钠的物质的量,计算样品中碳酸钠的质量,再利用质量分数的定义计算.
(2)实验装置中会残留部分二氧化碳,影响丁中二氧化碳质量的测定,需要通入空气将装置内的二氧化碳完全排入丁中被吸收,空气中含有二氧化碳,故应先用氢氧化钠溶液吸收,防止影响二氧化碳的测定;
空气中二氧化碳、水蒸气进入丁中影响二氧化碳的质量测定,导致测定二氧化碳的质量增大,戊装置的作用是吸收二氧化碳中的水蒸气,防止进入装置丁中;
(3)装置中含有二氧化碳,不将二氧化碳排尽,会使测定的二氧化碳的质量增大,故反应前应先通空气,排尽装置内的二氧化碳;
装置甲中二氧化碳与氢氧化钠反应生成碳酸钠与水;
(4)从装置乙中产生导出的气体中含有水,如果不除去气体中的水,会使丁中测定的二氧化碳的质量增大,故加入装置丁的二氧化碳应干燥,故装置丙中盛放的试剂是浓硫酸;
(5)由题意可知,反应生成的二氧化碳的质量为(w-m)g,计算二氧化碳的物质的量,根据碳元素守恒二氧化碳的物质的量等于样品中碳酸钠的物质的量,计算样品中碳酸钠的质量,再利用质量分数的定义计算.
解答:解:(1)装稀硫酸的装置是分液漏斗,故答案为:分液漏斗;
(2)实验装置中会残留部分二氧化碳,影响丁中二氧化碳质量的测定,需要通入空气将装置内的二氧化碳完全排入丁中被吸收,空气中含有二氧化碳,故应先用氢氧化钠溶液吸收,防止影响二氧化碳的测定,装置甲的作用是吸收空气中的二氧化碳;
空气中二氧化碳、水蒸气进入丁中影响二氧化碳的质量测定,导致测定二氧化碳的质量增大,戊装置的作用是吸收二氧化碳中的水蒸气,防止进入装置丁中,
故答案为:吸收空气中的二氧化碳;吸收二氧化碳中的水蒸气,防止进入装置丁中;
(3)装置中含有二氧化碳,不将二氧化碳排尽,会使测定的二氧化碳的质量增大,故反应前应先通空气,排尽装置内的二氧化碳,装置乙的作用是排出装置中的二氧化碳气体;
装置甲中二氧化碳与氢氧化钠反应生成碳酸钠与水,反应的离子方程式为CO2+2OH-=CO32-+H2O,
故答案为:排出装置中的二氧化碳气体;CO2+2OH-=CO32-+H2O;
(4)从装置乙中产生导出的气体中含有水,如果不除去气体中的水,会使丁中测定的二氧化碳的质量增大,导致测定的样品中碳酸钠的质量增大,测定的碳酸钠质量分数偏大.
故加入装置丁的二氧化碳应干燥,故装置丙中盛放的试剂是浓硫酸,
故答案为:浓硫酸;偏大;
(5)由题意可知,反应生成的二氧化碳的质量为(w-m)g,二氧化碳的物质的量为
=
mol,根据碳元素守恒可知样品中碳酸钠的物质的量为
mol,样品中碳酸钠的质量为
mol×106g/mo=
g,样品中碳酸钠质量分数为
×100%=
×100%,
故答案为:
×100%.
(2)实验装置中会残留部分二氧化碳,影响丁中二氧化碳质量的测定,需要通入空气将装置内的二氧化碳完全排入丁中被吸收,空气中含有二氧化碳,故应先用氢氧化钠溶液吸收,防止影响二氧化碳的测定,装置甲的作用是吸收空气中的二氧化碳;
空气中二氧化碳、水蒸气进入丁中影响二氧化碳的质量测定,导致测定二氧化碳的质量增大,戊装置的作用是吸收二氧化碳中的水蒸气,防止进入装置丁中,
故答案为:吸收空气中的二氧化碳;吸收二氧化碳中的水蒸气,防止进入装置丁中;
(3)装置中含有二氧化碳,不将二氧化碳排尽,会使测定的二氧化碳的质量增大,故反应前应先通空气,排尽装置内的二氧化碳,装置乙的作用是排出装置中的二氧化碳气体;
装置甲中二氧化碳与氢氧化钠反应生成碳酸钠与水,反应的离子方程式为CO2+2OH-=CO32-+H2O,
故答案为:排出装置中的二氧化碳气体;CO2+2OH-=CO32-+H2O;
(4)从装置乙中产生导出的气体中含有水,如果不除去气体中的水,会使丁中测定的二氧化碳的质量增大,导致测定的样品中碳酸钠的质量增大,测定的碳酸钠质量分数偏大.
故加入装置丁的二氧化碳应干燥,故装置丙中盛放的试剂是浓硫酸,
故答案为:浓硫酸;偏大;
(5)由题意可知,反应生成的二氧化碳的质量为(w-m)g,二氧化碳的物质的量为
| (w-m)g |
| 44g/mol |
| w-m |
| 44 |
| w-m |
| 44 |
| w-m |
| 44 |
| 53(w-m) |
| 22 |
| ||
| ng |
| 53(w-m) |
| 22n |
故答案为:
| 53(w-m) |
| 22n |
点评:本题考查学生对实验原理及装置理解、对操作的评价、物质含量的测定、化学计算等,难度中等,根据物质的化学性质,要认真分析,把握实验设计的每个步骤中的实验目的.

练习册系列答案
相关题目
对工业上的“三酸二碱”(硝酸、盐酸、硫酸、纯碱和烧碱),下列有关说法不正确的是( )
| A、室温下在浓硝酸、浓盐酸和浓硫酸中分别投入光亮的铁钉,在盐酸中溶解最快 | B、在氯碱工业中,产物烧碱在阴极区得到,两极气态产物可用于合成盐酸 | C、纯碱可用于生产普通玻璃;硝酸可用于制化肥和炸药等 | D、工业盐酸和工业硝酸都常呈黄色,因所含杂质完全相同 |
(12分)碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)工业上常用一定浓度的纯碱溶液清洗铁屑,目的是 。
(2)加入少量NaHCO3的目的是调节溶液的pH至 a,a的范围是 。
(3)已知室温下,Al(OH)3的Ksp=1.3×10-33,当pH=5时,溶液中c(Al3+)=
(4)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若参与反应的O2有11.2L(标准状况),则相当于节约NaNO2的物质的量为 ;O2参与反应的离子方程式为
(5)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)42+聚合离子。该水解反应的离子方程式为 。
(12分)碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
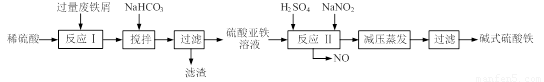
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
|
沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Al(OH)3 |
|
开始沉淀 |
2.3 |
7.5 |
3.4 |
|
完全沉淀 |
3.2 |
9.7 |
4.4 |
回答下列问题:
(1)工业上常用一定浓度的纯碱溶液清洗铁屑,目的是 。
(2)加入少量NaHCO3的目的是调节溶液的pH至 a,a的范围是 。
(3)已知室温下,Al(OH)3的Ksp=1.3×10-33,当pH=5时,溶液中c(Al3+)=
(4)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若参与反应的O2有11.2L(标准状况),则相当于节约NaNO2的物质的量为 ;O2参与反应的离子方程式为
(5)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)42+聚合离子。该水解反应的离子方程式为 。