题目内容
目前,大部分食盐用来生产氯气、氢气、烧碱和纯碱,进一步加工成各种含氯含钠的制品.如盐酸、漂粉精、氯化铁和聚氯乙烯等.根据所学知识,完成下列填空:
(1)以食盐为原料,生产氯气、氢气、烧碱的反应方程式是
(2)工业上常用氢气和氯气化合制取氯化氢气体.如图1是氢气和氯气化合的合成塔,其燃烧器的A管应通入
(3)如图2,用有阳离子交换膜(只允许阳离子通过)的立式隔膜电解槽电解食盐水时,精制饱和氯化钠溶液从
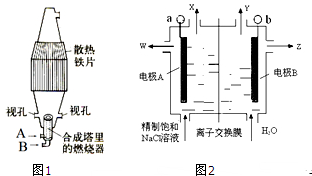
式是
(4)工业上以粗食盐(含有少量Ca2+、Mg2+杂质)、氨、石灰石等为原料,可以制备Na2CO3.其过程如图所示:
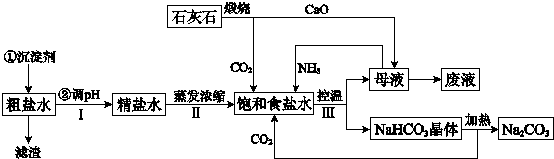
在处理粗盐水的过程中,可加入石灰乳和纯碱作为沉淀剂,则所得滤渣的成分除过量的沉淀剂外还有
(5)接(4)题,产品纯碱中常含有NaCl.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b g固体.则该产品中Na2CO3的质量分数是
分析:(1)氯碱工业:电解饱和食盐水得到氢氧化钠、氯气和氢气,该过程被人们称为中国现代化工之母;
(2)氯气有毒能污染环境,从A管中通入氢气可以将氯气包围,使氯气充分反应,减小污染环境;
(3)电解饱和食盐水阳极氯离子放电析出,需要定时补充氯离子,铁电极为阴极,电极反应式:O2+2H2O+4e-→4OH-;
(4)钙离子会与碳酸根离子生成沉淀,Ca2++CO32-=CaCO3↓,镁离子会与氢氧根离子生成沉淀,Mg2++2OH-=Mg(OH)2↓;
因二氧化碳在水中的溶解度小,氨气极易溶于水,所以,向饱和食盐水中首先通入氨气体,碳酸氢钠的溶解度小,利用浓碳酸氢铵溶液与氯化钠固体发生复分解反应;
(5)根据碳酸钠和盐酸反应的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑,找出碳酸钠和氯化钠之间的量的关系求解.
(2)氯气有毒能污染环境,从A管中通入氢气可以将氯气包围,使氯气充分反应,减小污染环境;
(3)电解饱和食盐水阳极氯离子放电析出,需要定时补充氯离子,铁电极为阴极,电极反应式:O2+2H2O+4e-→4OH-;
(4)钙离子会与碳酸根离子生成沉淀,Ca2++CO32-=CaCO3↓,镁离子会与氢氧根离子生成沉淀,Mg2++2OH-=Mg(OH)2↓;
因二氧化碳在水中的溶解度小,氨气极易溶于水,所以,向饱和食盐水中首先通入氨气体,碳酸氢钠的溶解度小,利用浓碳酸氢铵溶液与氯化钠固体发生复分解反应;
(5)根据碳酸钠和盐酸反应的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑,找出碳酸钠和氯化钠之间的量的关系求解.
解答:解:(1)人们将氯碱工业称为中国现代化工之母,电解方程式为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑,故答案为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑;氯碱工业;
(2)氯气有毒能污染环境,从A管中通入氢气可以将氯气包围,使氯气充分反应,减小污染环境,故答案为:H2;将氯气包围,使氯气充分反应,减小污染环境;
(3)电解饱和食盐水阳极氯离子放电析出,氯离子浓度减小,需要定时补充氯离子,铁电极为阴极,电极反应式:O2+2H2O+4e-→4OH-,故答案为阳极O2+2H2O+4e-→4OH-;
(4)钙离子会与碳酸根离子生成沉淀,Ca2++CO32-=CaCO3↓,镁离子会与氢氧根离子生成沉淀,Mg2++2OH-=Mg(OH)2↓,因二氧化碳在水中的溶解度小,氨气极易溶于水,所以,向饱和食盐水中首先通入氨气体,碳酸氢钠的溶解度小,利用浓碳酸氢铵溶液与氯化钠固体发生复分解反应,
故答案为:CaCO3、Mg(OH)2;NH3+H2O+CO2+NaCl=NaHCO3↓+NH4Cl;
(5)产品纯碱中常含有NaCl,取a g混合物与足量稀盐酸充分反应,Na2CO3+2HCl=2NaCl+H2O+CO2↑,得b g固体为NaCl,设碳酸钠的物质的量为X,
根据方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑
1 2
X 2x
混合物质量:117x+a-106X=b,X=
mol,该产品中Na2CO3的质量分数
×100%,
故答案为:
.
| ||
| ||
(2)氯气有毒能污染环境,从A管中通入氢气可以将氯气包围,使氯气充分反应,减小污染环境,故答案为:H2;将氯气包围,使氯气充分反应,减小污染环境;
(3)电解饱和食盐水阳极氯离子放电析出,氯离子浓度减小,需要定时补充氯离子,铁电极为阴极,电极反应式:O2+2H2O+4e-→4OH-,故答案为阳极O2+2H2O+4e-→4OH-;
(4)钙离子会与碳酸根离子生成沉淀,Ca2++CO32-=CaCO3↓,镁离子会与氢氧根离子生成沉淀,Mg2++2OH-=Mg(OH)2↓,因二氧化碳在水中的溶解度小,氨气极易溶于水,所以,向饱和食盐水中首先通入氨气体,碳酸氢钠的溶解度小,利用浓碳酸氢铵溶液与氯化钠固体发生复分解反应,
故答案为:CaCO3、Mg(OH)2;NH3+H2O+CO2+NaCl=NaHCO3↓+NH4Cl;
(5)产品纯碱中常含有NaCl,取a g混合物与足量稀盐酸充分反应,Na2CO3+2HCl=2NaCl+H2O+CO2↑,得b g固体为NaCl,设碳酸钠的物质的量为X,
根据方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑
1 2
X 2x
混合物质量:117x+a-106X=b,X=
| b-a |
| 11 |
| 106(b-a) |
| 11a |
故答案为:
| 106(b-a) |
| 11a |
点评:本题以氯碱工业为情境,考查了电解原理,粗盐精制等工艺流程,侧重于氯碱工业的考查,注意阳离子交换膜为解答该题的关键,注意审题,题目难度中等.

练习册系列答案
相关题目