题目内容
【题目】氮及其化合物与生产生活关系密切。请完成下列填空:
(1)某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验。
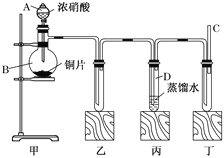
①装置甲中盛放浓硝酸的仪器A的名称是______, 装置丙中的试管内发生反应的离子方程式为:_______________________。
②为了探究NO的还原性,可以在装置丁的导气管C中通入一种气体,通入的这种气体的名称是____________。
(2)NO在医疗上有重要的应用,曾被科学家作为研究的重要物质。现有容积为aL的试管盛满NO后倒扣于水槽中,再向试管中通入一定体积O2后,试管内气体的体积为试管容积的一半,则通入的O2的在相同条件下体积为_________。
A 0.75aL B 0.375aL C 0.625aL D 1.25aL
(3)实验室常用下图所示装置制取并收集氨气。

①实验室制取氨气反应的化学方程式为____________________________________;
②图中方框内收集氨气的装置可选用_________________(填字母序号);
③尾气处理装置中使用倒扣漏斗的作用是_________________________________。
(4)在盛有一定量浓硝酸的试管中加入6.4g的铜片发生反应。请回答下列问题:
①开始阶段,反应的化学方程式为____________________________________,后一阶段生成气体的颜色为____________,若整个反应过程共产生标准状况下气体2.24L,则反应过程中被还原的HNO3的物质的量为_______。
②反应结束后铜片有剩余,再加入少量20%的稀硫酸,这时铜片上又有气泡产生,反应的离子方程式为____________________________________________________。
【答案】 分液漏斗 3NO2+H2O===2H++2NO![]() +NO 氧气 BD Ca(OH)2+2NH4Cl
+NO 氧气 BD Ca(OH)2+2NH4Cl ![]() CaCl2+2H2O+2NH3↑ C 防止烧杯中的水倒吸 Cu+4HNO3(浓)=Cu(NO)3+2NO2↑+2H2O 无色 0.1mol 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
CaCl2+2H2O+2NH3↑ C 防止烧杯中的水倒吸 Cu+4HNO3(浓)=Cu(NO)3+2NO2↑+2H2O 无色 0.1mol 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
【解析】(1)根据仪器A的结构特点知,A为分液漏斗;装置丙中的试管内二氧化氮与水反应生成硝酸和一氧化氮,发生反应的离子方程式为:3NO2+H2O=2H++2NO![]() +NO;②为了探究NO的还原性,可以在装置丁的导气管C中通入氧气,无色气体变为红棕色,发生反应2NO+O2= 2NO2;(2)容积为aL的试管盛满NO后倒扣于水槽中,再向试管中通入一定体积O2后,试管内气体的体积为试管容积的一半,发生的反应为:①2NO+O2=2NO2,②3NO2+H2O=2HNO3+NO,合并反应为③4NO+3O2+2H2O=4HNO3,若反应后试管内的气体为NO,体积为
+NO;②为了探究NO的还原性,可以在装置丁的导气管C中通入氧气,无色气体变为红棕色,发生反应2NO+O2= 2NO2;(2)容积为aL的试管盛满NO后倒扣于水槽中,再向试管中通入一定体积O2后,试管内气体的体积为试管容积的一半,发生的反应为:①2NO+O2=2NO2,②3NO2+H2O=2HNO3+NO,合并反应为③4NO+3O2+2H2O=4HNO3,若反应后试管内的气体为NO,体积为![]() L,则按反应③计算,则通入的O2体积为
L,则按反应③计算,则通入的O2体积为![]() L×
L×![]() =0.375aL;若反应后试管内的气体为O2,体积为
=0.375aL;若反应后试管内的气体为O2,体积为![]() L,则按反应③计算,则通入的O2体积为
L,则按反应③计算,则通入的O2体积为![]() L+aL×
L+aL×![]() =1.25aL;答案选BD;(3)①实验室利用熟石灰与氯化铵加热反应制取氨气,反应的化学方程式为:Ca(OH)2+2NH4Cl
=1.25aL;答案选BD;(3)①实验室利用熟石灰与氯化铵加热反应制取氨气,反应的化学方程式为:Ca(OH)2+2NH4Cl ![]() CaCl2+2H2O+2NH3↑;②氨气极易溶于水,密度比空气小,所以收集氨气可选用向下排空气法,根据进气方向应该用C装置; ③氨气极易溶于水,倒置漏斗有缓冲作用,气体能充分被吸收且防止烧杯中的水倒吸;(4)①开始阶段,铜片与浓硝酸反应生成硝酸铜、二氧化氮和水,反应的化学方程式为:Cu+4HNO3(浓)=Cu(NO)3+2NO2↑+2H2O;随着反应的进行,浓硝酸逐渐变稀,后一阶段为稀硝酸与铜片反应,生成无色气体一氧化氮;若整个反应过程共产生标准状况下气体2.24L,根据氮原子守恒,则反应过程中被还原的HNO3的物质的量为n(HNO3)=n(NOx)=
CaCl2+2H2O+2NH3↑;②氨气极易溶于水,密度比空气小,所以收集氨气可选用向下排空气法,根据进气方向应该用C装置; ③氨气极易溶于水,倒置漏斗有缓冲作用,气体能充分被吸收且防止烧杯中的水倒吸;(4)①开始阶段,铜片与浓硝酸反应生成硝酸铜、二氧化氮和水,反应的化学方程式为:Cu+4HNO3(浓)=Cu(NO)3+2NO2↑+2H2O;随着反应的进行,浓硝酸逐渐变稀,后一阶段为稀硝酸与铜片反应,生成无色气体一氧化氮;若整个反应过程共产生标准状况下气体2.24L,根据氮原子守恒,则反应过程中被还原的HNO3的物质的量为n(HNO3)=n(NOx)= ![]() =0.1mol;②随着反应的进行,浓硝酸组建变为稀硝酸,Cu片和稀硝酸也会发生这一反应,化学反应方程式:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,离子方程式为:3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑,由上面两个离子方式可以看出,溶液中的H+消耗完之后溶液中仍然有NO3-剩余,所以这时候加硫酸提供了H+,又相当于稀硝酸的溶液,所以又会发生铜片与稀硝酸的反应,离子方程式:3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑。
=0.1mol;②随着反应的进行,浓硝酸组建变为稀硝酸,Cu片和稀硝酸也会发生这一反应,化学反应方程式:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,离子方程式为:3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑,由上面两个离子方式可以看出,溶液中的H+消耗完之后溶液中仍然有NO3-剩余,所以这时候加硫酸提供了H+,又相当于稀硝酸的溶液,所以又会发生铜片与稀硝酸的反应,离子方程式:3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑。

 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案