题目内容
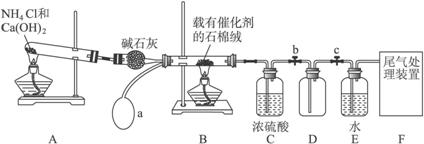
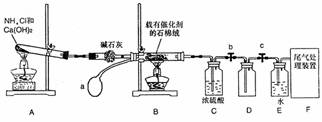
下列仪器和装置,用橡胶管经过简单连接,可制备收集多种不同的气体(暂不考虑尾气吸收).关于这些装置的连接,下列说法正确的是

- A.制备收集C2H4:连接a→d→f
- B.制备收集NO2,连接a→c→f
- C.制备收集H2S,连接b→c→e
- D.制备收集NH3,连接b→d→e
D
分析:A.实验室制备乙烯所用的原料为乙醇,浓硫酸作催化剂、脱水剂,反应条件是加热到170℃,据此选择实验装置;
B.实验室制备NO2,所用的原料为铜和浓硝酸,反应生成硝酸铜、二氧化氮和水,据此选择实验装置;
C.实验室制备H2S,所用的原料为硫化亚铁(FeS)固体和稀盐酸,反应生成氯化亚铁和硫化氢,据此选择实验装置;
D.实验室制备NH3,可用浓氨水和CaO固体反应,反应生成氢氧化钙和氨气,据此选择实验装置;
解答:A.实验室制备乙烯,利用乙醇在浓硫酸的催化作用下发生分子内脱水制取乙烯,乙醇发生了消去反应:CH3CH2OH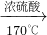 CH2=CH2↑+H2O,所以需温度计测在反应混合物中测量反应的温度,否则发生其它副反应,所以连接a→d→f无法制备,故A错误;
CH2=CH2↑+H2O,所以需温度计测在反应混合物中测量反应的温度,否则发生其它副反应,所以连接a→d→f无法制备,故A错误;
B.实验室制备NO2,利用铜和浓硝酸反应生成硝酸铜、二氧化氮和水,方程式为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,反应无需加热,所以不能选择a装置,二氧化氮和水反应生成一氧化氮和硝酸,所以二氧化氮不能用排水法收集,所以连接a→c→f无法制备,故B错误;
C.实验室制备H2S,利用硫化亚铁(FeS)固体和稀盐酸反应生成氯化亚铁和硫化氢,其化学方程式为 FeS+2HCl═FeCl2+H2S↑,制取H2S的反应物为固体和液体反应不需要加热,可选择b装置,但硫化氢具有还原性,浓硫酸具有强氧化性,两者发生氧化还原反应,H2S+H2SO4(浓)=SO2+S↓+2H2O,所以不能选C装置,所以连接连接b→c→e无法制备,故C错误;
D.实验室制备NH3,可用浓氨水和CaO固体反应,NH3?H2O+CaO═Ca(OH)2+NH3↑,浓氨水易挥发,CaO固体与水反应放出大量的热,导致温度升高,使得氨气在水中的溶解度进一步减少,以气体的形式逸出,制得氨气,可选择b装置,制得的氨气中含有水蒸气,可用碱石灰干燥,氨气密度比空气小,需用向下排空气法收集,所以需短管进,长管出,所以连接b→d→e可制备收集氨气,故D正确;
故选D.
点评:本题主要考查了实验室制备乙烯、NO2、H2S、NH3,掌握它们的制备原理是解答的关键,题目难度中等.
分析:A.实验室制备乙烯所用的原料为乙醇,浓硫酸作催化剂、脱水剂,反应条件是加热到170℃,据此选择实验装置;
B.实验室制备NO2,所用的原料为铜和浓硝酸,反应生成硝酸铜、二氧化氮和水,据此选择实验装置;
C.实验室制备H2S,所用的原料为硫化亚铁(FeS)固体和稀盐酸,反应生成氯化亚铁和硫化氢,据此选择实验装置;
D.实验室制备NH3,可用浓氨水和CaO固体反应,反应生成氢氧化钙和氨气,据此选择实验装置;
解答:A.实验室制备乙烯,利用乙醇在浓硫酸的催化作用下发生分子内脱水制取乙烯,乙醇发生了消去反应:CH3CH2OH
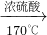 CH2=CH2↑+H2O,所以需温度计测在反应混合物中测量反应的温度,否则发生其它副反应,所以连接a→d→f无法制备,故A错误;
CH2=CH2↑+H2O,所以需温度计测在反应混合物中测量反应的温度,否则发生其它副反应,所以连接a→d→f无法制备,故A错误;B.实验室制备NO2,利用铜和浓硝酸反应生成硝酸铜、二氧化氮和水,方程式为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,反应无需加热,所以不能选择a装置,二氧化氮和水反应生成一氧化氮和硝酸,所以二氧化氮不能用排水法收集,所以连接a→c→f无法制备,故B错误;
C.实验室制备H2S,利用硫化亚铁(FeS)固体和稀盐酸反应生成氯化亚铁和硫化氢,其化学方程式为 FeS+2HCl═FeCl2+H2S↑,制取H2S的反应物为固体和液体反应不需要加热,可选择b装置,但硫化氢具有还原性,浓硫酸具有强氧化性,两者发生氧化还原反应,H2S+H2SO4(浓)=SO2+S↓+2H2O,所以不能选C装置,所以连接连接b→c→e无法制备,故C错误;
D.实验室制备NH3,可用浓氨水和CaO固体反应,NH3?H2O+CaO═Ca(OH)2+NH3↑,浓氨水易挥发,CaO固体与水反应放出大量的热,导致温度升高,使得氨气在水中的溶解度进一步减少,以气体的形式逸出,制得氨气,可选择b装置,制得的氨气中含有水蒸气,可用碱石灰干燥,氨气密度比空气小,需用向下排空气法收集,所以需短管进,长管出,所以连接b→d→e可制备收集氨气,故D正确;
故选D.
点评:本题主要考查了实验室制备乙烯、NO2、H2S、NH3,掌握它们的制备原理是解答的关键,题目难度中等.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目


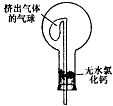
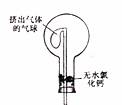 ①用烧瓶收集满干燥的氨气,立即塞上如图的示的橡胶塞。
①用烧瓶收集满干燥的氨气,立即塞上如图的示的橡胶塞。