题目内容
【题目】某学习小组利用下列装置探究氯气与氨气的反应.其中A、B分别为氯气和氨气的发生装置,C为纯净干燥的氯气与氨气反应的装置.
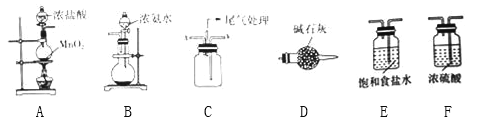
(1)若Cl2从左向右流动,NH3从右向左流动,则上述实验装置中,依次连接的合理顺序为:A→________________→B;为使NH3与Cl2更充分混合,Cl2应从C装置的__口进入(填“x”或“y”).
(2)简述装置A中使用分液漏斗向圆底烧瓶中滴加浓盐酸的操作是__________________.
(3)装置A中发生反应的离子方程式为_______________________________.
(4)装置B中圆底烧瓶内的试剂为______________(填名称).
(5)装置D的作用是____________________________.
(6)反应开始后,装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气中的主要成分之一,该反应的化学方程式为________________________________
【答案】 E、F、C、D x 打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,缓慢滴加 MnO2+4H++2C1﹣![]() Mn2++C12↑+2H2O 氢氧化钠固体、碱石灰或生石灰等 吸收水蒸气,干燥氨气 3Cl2+8NH3═N2+6NH4Cl
Mn2++C12↑+2H2O 氢氧化钠固体、碱石灰或生石灰等 吸收水蒸气,干燥氨气 3Cl2+8NH3═N2+6NH4Cl
【解析】(1)Cl2从左向右流动,NH3从右向左流动,A是氯气的发生装置,产生氯气后,用饱和食盐水吸收氯气中混有的HCl气体,再用浓硫酸干燥,制备纯净干燥的氯气;B装置是氨气的发生装置,产生氨气后,用碱石灰干燥;制得氯气和氨气在C装置中发生反应,所以上述实验装置中,依次连接的合理顺序为:A→E→F→C→D→B;由于Cl2密度比空气的密度大,为使NH3与Cl2更充分混合,Cl2应从C装置的x口进入;
(2)装置A中使用分液漏斗向圆底烧瓶中滴加浓盐酸的操作是打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,缓慢滴加;
(3)装置A中是制备氯气的发生装置,是在加热的条件下进行的反应,所用原料为二氧化锰和浓盐酸,离子方程式为:MnO2+4H++2C1﹣![]() Mn2++C12↑+2H2O;
Mn2++C12↑+2H2O;
(4)装置B是在常温下进行的反应,可以和浓氨水产生氨气的试剂可以是氢氧化钠固体、碱石灰或生石灰等,所以圆底烧瓶内的试剂为氢氧化钠固体、碱石灰或生石灰等;
(5)装置D主要用于吸收水蒸气,干燥氨气;
(6)反应开始后,装置C内出现浓厚的白烟并在容器内壁凝结,推测此物质为氯化铵固体,
另一生成物是空气中的主要成分之一,即氮气,因此该反应的化学方程式为:3Cl2+8NH3═N2+6NH4Cl。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案【题目】现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复).
阳离子 | H+、Na+、A13+、Ag+、Ba2+ |
阴离子 | OH﹣、Cl﹣、CO |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性;
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生;
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀;
④上述沉淀包括难溶物和微溶物
(1)将C溶液逐滴加入等体积、等物质的量的浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为: .
(2)写出E溶液与过量的B溶液反应的离子方程式 .
(3)已知:NaOH(aq)+HNO3(aq)═NaNO3(aq)+H2O(l);△H=﹣akJmol﹣1 . 请写出B与C的稀溶液反应的热化学方程式 .
(4)在100mL 0.1 molL﹣1E溶液中,逐滴加入35 mL 2 molL﹣1NaOH溶液,最终得到沉淀的物质的量为 .




