题目内容
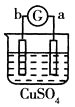
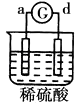
【题目】某小组为研究电化学原理,设计如图装置。下列叙述不正确的是( )

A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu
C. 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色
D. a和b用导线连接时,Fe片上发生还原反应,溶液中SO42-向铜电极移动
【答案】D
【解析】分析:a和b不连接时,不能构成原电池,铁与硫酸铜发生置换反应生成硫酸亚铁和铜;a和b用导线连接时,构成原电池,铁是负极,铜是正极,结合选项分析判断。
详解:A.a和b不连接时,由于金属活动性Fe>Cu,所以在铁片上会发生反应:Fe+Cu2+=Fe2++Cu,在铁片有金属铜析出,A正确;
B.a和b用导线连接时,形成了原电池,Cu作原电池的正极,在铜片上发生的反应为:Cu2++2e-=Cu,B正确;
C.无论a和b是否连接,Fe都会失去电子,变为Fe2+,而Cu2+会得到电子变为Cu,所以铁片均会溶解,溶液从蓝色逐渐变成浅绿色,C正确;
D.a和b用导线连接后,铁作负极,铜作正极,铁片上发生氧化反应,溶液中硫酸根离子向铁电极移动,D错误。答案选D。

 口算能手系列答案
口算能手系列答案【题目】如下图所示的装置中,观察到电流计指针偏转,M棒变粗,N棒变细,并测得电解质溶液的质量减小,由此判断下表中所列M、N、P物质,其中可以成立的是( )

M | N | P | |
A | Zn | Cu | 稀硫酸溶液 |
B | Cu | Fe | 稀盐酸 |
C | Ag | Zn | 硝酸银溶液 |
D | Zn | Fe | 硫酸亚铁溶液 |
A. A B. B C. C D. D
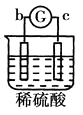
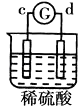
【题目】有a、b、c、d四个金属电极,G为电流计,有关的反应装置及部分反应现象记录如下:
实验 |
|
|
|
|
部分实 | a极质量减小 | 溶液中的SO42﹣﹣向b极移动 | d极溶解c极 | 电子从d极 |
由此可判断这四种金属的活动性顺序是( )
A.d>a>b>c
B.a>b>c>d
C.b>c>d>a
D.a>b>d>c