题目内容
请完成下列各题:
(1)前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有 种。
(2)第ⅢA、ⅤA原元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为 。在GaN晶体中,每个Ga原子与 个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为 。在四大晶体类型中,GaN属于 晶体。
(3)在极性分子NCl3中,N原子的化合物为―3,Cl原子的化合价为+1,请推测NCl3水解的主要产物是 (填化学式)。
答案:(1)5
(2)1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1) 4 正四面体 原子
(3)HClO NH3·H2O
(1)第四周期中,基态原子中未成对电子数与其周期数相同的元素包括:第1周期的氢、第二周期的碳和氧、第三周期的磷、第四周期的铁,共5种。
(2)Ga在元素周期表中是第四周期、第ⅢA族,原子序数是31,即其原子核外电子数是31,根据核外电子的排布规律可以写出该原子的电子排布式为:1s22s22p63s23p63d104s24p1或[Ar]3d104s24p1。因为GaN晶体结构与单晶硅相似,可知GaN晶体是原子晶体,晶体结构为空间网状结构,每个Ga原子与四个N相连,这四个N原子构成的空间构型是正四面体型。
(3)水解反应前后各元素的化合价不变,由题意知NCl3中N的化合价为-3价,Cl的化合价为+1价,则在NCl3水解的产物中N的化合价也是-3价,Cl的化合价是+1价,分析可知其水解产物是HClO和NH3 ·H2O 。

练习册系列答案
相关题目
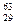 Cu和
Cu和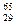 Cu,参考铜的原子量(63.5)估算
Cu,参考铜的原子量(63.5)估算