题目内容
铜和稀硝酸可以发生下列反应:Cu+HNO3(稀)--Cu(NO3)2+NO↑+H2O
(1)配平上述反应,并用双线桥标出电子转移的方向和数目.
Cu+ HNO3(稀)- Cu(NO3)2+ NO↑+ H2O
(2)其中还原产物是 ;稀HNO3在反应中的作用有 .
(3)若消耗0.2mol氧化剂,则被氧化的还原剂的物质的量是 ,转移电子的数目为: .
(1)配平上述反应,并用双线桥标出电子转移的方向和数目.
(2)其中还原产物是
(3)若消耗0.2mol氧化剂,则被氧化的还原剂的物质的量是
考点:氧化还原反应
专题:氧化还原反应专题
分析:(1)该反应中Cu元素化合价由0价变为+2价、N元素化合价由+5价变为+2价,根据转移电子相等、原子守恒配平方程式;
(2)该反应中硝酸是氧化剂,其对应的产物是还原产物,根据硝酸中N元素化合价是否变化确定稀释的性质;
(3)根据氧化剂和还原剂之间的关系式、氧化剂和转移电子之间的关系式计算.
(2)该反应中硝酸是氧化剂,其对应的产物是还原产物,根据硝酸中N元素化合价是否变化确定稀释的性质;
(3)根据氧化剂和还原剂之间的关系式、氧化剂和转移电子之间的关系式计算.
解答:
解:(1)该反应中Cu元素化合价由0价变为+2价、部分N元素化合价由+5价变为+2价,其得失电子最小公倍数是6,
用双线桥标出该反应电子转移的方向和数目为 ,
,
故答案为:3;8;3;2;4; ;
;
(2)该反应中氧化剂是硝酸,则还原产物是NO,该反应中部分N元素化合价不变、部分N元素化合价由+5价变为+2价,则硝酸体现酸性和氧化性,故答案为:NO;酸性和氧化性;
(3)该反应中有
的硝酸作氧化剂,则氧化剂和还原剂的物质的量之比为2:3,如果消耗0.2mol氧化剂,则被氧化的还原剂的物质的量是0.3mol,转移电子数=0.2mol×3×NA/mol=0.6NA,故答案为:0.3mol;0.6NA.
用双线桥标出该反应电子转移的方向和数目为
 ,
,故答案为:3;8;3;2;4;
 ;
;(2)该反应中氧化剂是硝酸,则还原产物是NO,该反应中部分N元素化合价不变、部分N元素化合价由+5价变为+2价,则硝酸体现酸性和氧化性,故答案为:NO;酸性和氧化性;
(3)该反应中有
| 1 |
| 4 |
点评:本题以硝酸和铜反应为载体考查了氧化还原反应,根据元素化合价变化确定硝酸的性质,再结合各个物理量之间的关系式计算,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法中,正确的是( )
| A、对“地沟油”进行分馏可以获得汽油发动机的燃料 |
| B、乙烯和聚乙烯都可与溴水发生加成反应 |
| C、研究表明禽流感病毒H7N9在沸水中两分钟就能被杀死,是因为蛋白质受热易变性 |
| D、乙醇和乙酸的反应与苯和液溴的反应类型不同 |
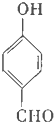 对基苯甲醛,…俗称PHBA,是-种重要的有机化工原料.其结构如图所示
对基苯甲醛,…俗称PHBA,是-种重要的有机化工原料.其结构如图所示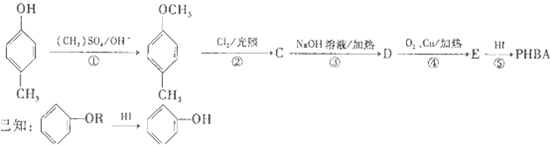
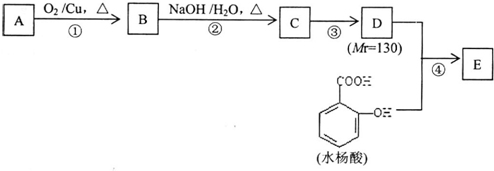
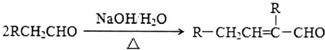

 Na、Fe、Cu、Al是常见的金属元素,请按要求回答下列问题:
Na、Fe、Cu、Al是常见的金属元素,请按要求回答下列问题: