题目内容
物质的制备方法可以分为实验室制法和工业制法。下列反应中既属于氧化还原反应又属于实验室制法的是
①制SO2:Na2S2O3+H2SO4 ="===" Na2SO4+H2O+SO2↑+S↓
②制氧气: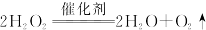
③制氯气: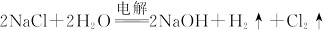
④制氨气: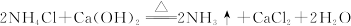
⑤制硝酸: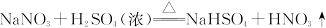
⑥制H2:Mg+H2SO4====MgSO4+H2↑
①制SO2:Na2S2O3+H2SO4 ="===" Na2SO4+H2O+SO2↑+S↓
②制氧气:
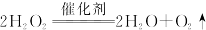
③制氯气:
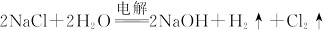
④制氨气:
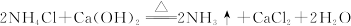
⑤制硝酸:
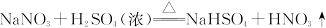
⑥制H2:Mg+H2SO4====MgSO4+H2↑
| A.①②③⑥ |
| B.② |
| C.②⑥ |
| D.全部 |
B
判断氧化还原反应的标准是:根据化合价是否有变化,所以排除④与⑤;实验室制取物质需要考虑反应条件、反应速率的快慢等方面因素,因此排除①、③、⑥。

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
 Fe2O3 + SO2↑+ SO3↑+ 14H2O。其中三氧化硫与水蒸气同时冷凝便得到硫酸。用如图所示装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去)。其中b为干燥的试管。下列关于该反应说法正确的是( )
Fe2O3 + SO2↑+ SO3↑+ 14H2O。其中三氧化硫与水蒸气同时冷凝便得到硫酸。用如图所示装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去)。其中b为干燥的试管。下列关于该反应说法正确的是( )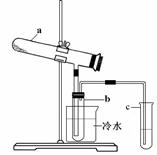
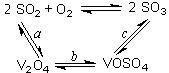
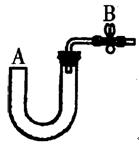
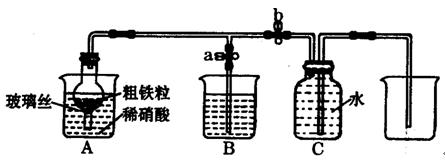
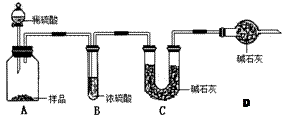
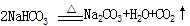 。请回答:
。请回答: 成 功
成 功 成 功
成 功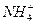 、
、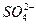 、Fe2+和结晶水,设计了下列操作步骤:①取少量该化合物加热,发现试管口处有液体,该液体能使无水硫酸铜变蓝;②另取少量该化合物溶于水中,滴加少量的氯水,再加入KSCN溶液,有血红色出现;③取少量溶液于试管中,加入盐酸,没有现象,再加入BaCl2溶液,有白色沉淀生成;④取少量溶液于试管中,加入浓的NaOH溶液,微热有使湿润的红色石蕊试纸变蓝的气体产生,同时也有白色沉淀产生,该沉淀很快变成灰绿色沉淀。
、Fe2+和结晶水,设计了下列操作步骤:①取少量该化合物加热,发现试管口处有液体,该液体能使无水硫酸铜变蓝;②另取少量该化合物溶于水中,滴加少量的氯水,再加入KSCN溶液,有血红色出现;③取少量溶液于试管中,加入盐酸,没有现象,再加入BaCl2溶液,有白色沉淀生成;④取少量溶液于试管中,加入浓的NaOH溶液,微热有使湿润的红色石蕊试纸变蓝的气体产生,同时也有白色沉淀产生,该沉淀很快变成灰绿色沉淀。