题目内容
16.设NA为阿伏加德罗常数的值,下列说法正确的是( )①1mol CH5+中含11NA个电子
②1mol-OH中含10NA个电子
③1mol Cl0H22分子中共价键总数为31NA
④0.4mol以任意比例混合的乙炔和乙醛气体在氧气中充分燃烧时,消耗氧分子数为NA
⑤1L 1mol•L-1苯酚钠溶液中含有C6H5O-的个数为NA?
⑥28g乙烯和环丙烷组成的混合气体中含有3NA个氢原子?
| A. | ①④ | B. | ②⑥ | C. | ③④ | D. | ②⑤ |
分析 ①CH5+中含10个电子;
②-OH不带电荷;
③Cl0H22分子中含9条C-C键和22条C-H键;
④等物质的量的乙炔和乙醛气体在氧气中充分燃烧时,消耗氧气的物质的量相等;
⑤C6H5O-为弱酸根,在溶液中会水解;
⑥乙烯和环丙烷的最简式均为CH2.
解答 解:①CH5+中含10个电子,故1molCH5+中含10mol电子即10NA个,故错误;
②-OH不带电荷,故1mol-OH中含9mol电子即9NA个,故错误;
③Cl0H22分子中含9条C-C键和22条C-H键,故1molCl0H22中含31mol共价键即31NA个,故正确;
④1mol乙炔和1mol乙醛气体在氧气中充分燃烧时,消耗氧气的物质的量相等,均为2.5mol,故0.4mol以任意比例混合的乙炔和乙醛气体在氧气中充分燃烧时,消耗氧分子数为NA,与乙炔和乙醛的比例无关,故正确;
⑤C6H5O-为弱酸根,在溶液中会水解,故溶液中含有C6H5O-的个数小于NA,故错误;
⑥乙烯和环丙烷的最简式均为CH2,故28g乙烯和环丙烷中含有的CH2的物质的量n=$\frac{28g}{14g/mol}$=2mol,即含4NA个氢原子,故错误.
故选C.
点评 本题考查阿伏加德罗常数的相关计算,题目难度不大,注意物质的组成、结构、性质以及物质存在的外界条件和聚集状态等问题,④为易错点.

练习册系列答案
相关题目
6.化学在资源利用、环境保护等与社会可持续发展密切相关的领域发挥着积极作用.下列做法与社会可持续发展理念相违背的是( )
| A. | 回收利用废旧金属 | B. | 吸收硫酸工业尾气 | ||
| C. | 大力开发不可再生资源 | D. | 改进汽车尾气净化技术 |
7.下列有机物命名正确的是( )
| A. | 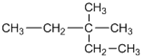 2-甲基-2-乙基甲烷 2-甲基-2-乙基甲烷 | B. | CH3C(CH3)2CH2CH3 2,2-二甲基丁烷 | ||
| C. | 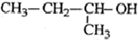 2-甲基-1-丙醇 2-甲基-1-丙醇 | D. | 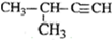 2-甲基-3-丁炔 2-甲基-3-丁炔 |
1.下列实验操作,处理方法错误的是( )
| A. | 做银镜反应的试管先用NaOH溶液洗涤,倒掉后再用清水冲洗干净 | |
| B. | 皮肤上若沾有少量的苯酚用酒精洗 | |
| C. | 做银镜反应后的试管一般采用浓盐酸洗涤 | |
| D. | 制乙烯的实验温度计应伸入液面下 |
8.下列叙述正确的是( )
| A. | 苯的分子式是C6H6,不能使酸性高锰酸钾溶液褪色,属于饱和烃 | |
| B. | 从苯的凯库勒式看,分子中含有双键,所以属于烯烃 | |
| C. | 乙烯可作果实的催熟剂 | |
| D. | 充分燃烧后产生二氧化碳和水的有机物就是烃 |
5.已知氧化性:Br2>Fe3+,在FeBr2溶液中通人Cl2,则所通人Cl2与FeBr2的物质的量之比和所发生的离子方程式对应关系错误的是.( )
| 选项 | n(Cl2)/n(FeBr2) | 离子方程式 |
| A | 1:1 | 2Cl2+2Fe3++2Br-=2Fe3++Br2+4Cl- |
| B | 2:1 | 3Cl2+2Fe2++4Br-=2Fe3++2Br2+6Cl- |
| C | 1:2 | Cl2+2Br-=Br2+2Cl- |
| D | 2:3 | 4Cl2+62Fe2++2Br-=6Fe3++Br2+8Cl- |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |

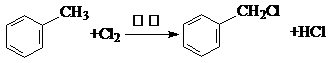 ;
;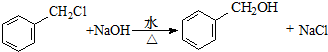 .
. 产生.请写出该反应的化学方程式:
产生.请写出该反应的化学方程式: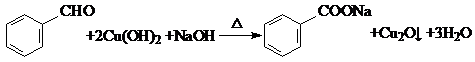 .
.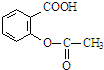 )、丁香油酚(
)、丁香油酚(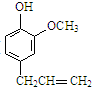 )在医学上具有广泛用途.
)在医学上具有广泛用途.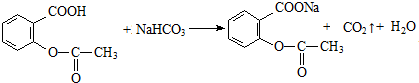 .
.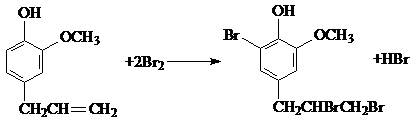 .
. .请写出以对苯二甲酸(
.请写出以对苯二甲酸(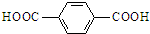 )和乙二醇为原料合成涤纶的化学方程式:
)和乙二醇为原料合成涤纶的化学方程式: