��Ŀ����
����Ŀ��ij�������ۺϴ�����NH4-��ˮ��ҵ��������Ҫ��N2��CO2��.SO2��NO��CO,�����������ɷ֣���������������̣�

��֪��NO+NO2+2NaOH=2NaNO2+H2O
�ش��������⣺
(1)����1����Ҫ�ɷ�Ca(OH)2��CaCO3��______��
(2)����X������1��Ӧʱ��������______(���������������ԭ����������������Ҳ���ǻ�ԭ��������������������������Ҫ��______ (�ѧʽ����
(3) NaOH��Һ���յ����ʵ�����NO��NO2��������У�������1molNaNO2ʱת�Ƶ�����Ϊ_______NA��
(4)��NaNO2��Һ������NH4-��ˮʱ��������Ӧ�����ӷ���ʽΪ__________����NH4-��ˮҲ���ó�����������Mg2++NH4- +PO43-=== MgNH4PO4��, ��֪25��ʱ��Ksp(MgNH4PO4)=2.5��10-13 �����ˮ�а�����Ͷ��þ�κ������Σ���ʹ�������ˮ�в������̬���ﵽһ���ŷű�(��1.0mg��L-1������7.14��10-5 mol��L-1������c(PO43-)=1.0��10-5 mol��L-1����Ӧʹ������ķ�ˮ��c( Mg2+) ��________��
(5)�绯ѧ�������Ǵ���������ˮ��һ���¹��ա���ӵ�������ԭ���ǣ����ˮ�м���һ�����������ӣ�ʹ����ʱ�������ŵ������ȵ��ʣ������ȵ�����ˮ��Ӧ���ɵĴ����ὫNH4+���� Ϊ���������һ����Ӧ�����ӷ���ʽΪ__________________________��
(6) ��֪25��ʱ��HNO2�ĵ��볣��Ks =5.1��10-4��ʵ���ҳ���NaOH��Һ����NO2β������ӦΪ2NO2+ 2NaOH==NaNO3+ NaNO2+H2O������1L 0.4 mol��L-1Na(OH)��Һ�������0.4mol NO2���壬��������Һ��___(����ԡ��������ԡ������ԡ�����ԭ����___________(�����ӷ���ʽ��ʾ����������Һ����仯�����Ƽ���������Һ��pH��____��
���𰸡� CaSO3 ������ CO 0.5 NH4++NO2��=N2��+2H2O 0.035 2NH4++3HClO = N2��+3Cl��+5H++3H2O ���� NO2��+H2O ![]() HNO2+OH�� 8.3��8+lg2��
HNO2+OH�� 8.3��8+lg2��
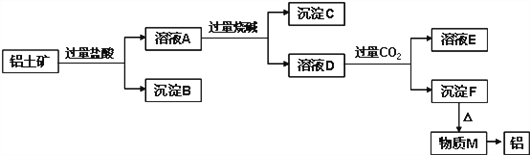
����������ҵ������CO2��SO2�ɱ�ʯ��ˮ���գ����ɷ���ΪCaCO3��CaSO3������1�Dz��ܱ�����ʯ��ˮ���յ�N2��NO��CO������1��ͨ�������������������Һ������NaNO2��ͨ����������ܹ���������õ������ƣ�NaNO2�뺬��NH4+����Һ��Ӧ��������Ⱦ���壬Ӧ���ɵ�����������2����CO��N2��������������������Ҫ��CO��
��1����ҵ������SO2�ɱ�ʯ��ˮ���գ�����CaSO3��CO2�ɱ�ʯ��ˮ���գ�����CaCO3�����������ƹ�����������ijɷ�Ϊ��Ҫ����Ca��OH��2��CaCO3��CaSO3��
��2��NO��O2��������ΪNO2��O2����������������������������������Ҫ��CO��
(3) NaOH��Һ���յ����ʵ�����NO��NO2���壬������ӦΪNO+NO2+2NaOH=2NaNO2+H2O��������1molNaNO2ʱ�μӷ�Ӧ��NOΪ0.5mol����ת�Ƶ�����Ϊ0.5NA��
��4����NaNO2��Һ������NH4+��ˮʱ��NH4+��NO2-�������з�Ӧ����N2�ͺ�ˮ�����ӷ�Ӧ����ʽΪNH4++NO2��=N2��+2H2O��Ksp(MgNH4PO4)=c(Mg2+)��c(NH4+)��c(PO43-)=c(Mg2+)��(7.14��10-5 mol��L-1)��(1.0��10-5 mol��L-1)=2.5��10-13 �����c( Mg2+) =0.035 mol��L-1��
(5)�����ὫNH4+����Ϊ������������ԭΪCl-������������ԭ��Ӧ�ĵ����غ㣬���������غ㡢ԭ���غ㣬�˷�Ӧ�����ӷ���ʽΪ2NH4++3HClO = N2��+3Cl��+5H++3H2O��
(6) ��1L 0.4 mol��L-1Na(OH)��Һ�������0.4mol NO2���壬��Ϸ�Ӧ2NO2+ 2NaOH==NaNO3+ NaNO2+H2O��֪ǡ����ȫ���գ�����Һ��NaNO2��NaNO3��0.2mol������Һ�д���NO2��+H2O![]() HNO2+OH����������Һ�Լ��ԣ����HNO2
HNO2+OH����������Һ�Լ��ԣ����HNO2![]() NO2-+H+����֪��[c(OH��)��c(HNO2)]��c(NO2��)=Kw��Ks����c(OH��)=c(HNO2)�����c(OH��)=2��10-6mol��L-1����ʱ��Һ��c(H+)=Kw��c(OH��)=5��10-9mol��L-1������Һ��pH=9-lg5=8.3��
NO2-+H+����֪��[c(OH��)��c(HNO2)]��c(NO2��)=Kw��Ks����c(OH��)=c(HNO2)�����c(OH��)=2��10-6mol��L-1����ʱ��Һ��c(H+)=Kw��c(OH��)=5��10-9mol��L-1������Һ��pH=9-lg5=8.3��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�