题目内容
如图为用酸性氢氧燃料电池为电源进行电解的实验装置示意图。下列说法中,正确的是
| A.燃料电池工作时,正极反应为:O2 + 4H++ 4e-= 2H2O |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a极是含锌、铁的粗铜,b极是纯铜,a极溶解铜的质量与b极析出铜的质量相等 |
| D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
A
解析试题分析:A、因为燃料电池的电解质呈酸性,正极反应为:O2 + 4H++ 4e-= 2H2O,正确;B、a极为阳极,逐渐溶解,b极为阴极,有铜析出,错误;C、因为a极Cu、Zn、Fe失电子,b极Cu2+得电子生成Cu,a极溶解铜的质量与b极析出铜的质量不相等,错误;D、a、b两极均是石墨时,根据电子守恒,a极产生产生O2,体积为电池中消耗的H2体积的1/2,错误。
考点:本题考查燃料电池、电解原理及应用。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
对于下图的锌锰电池,下列说法正确的是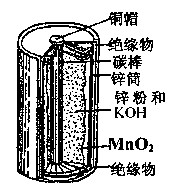
| A.MnO2是氧化剂,被氧化 |
| B.碳棒为负极、锌筒为正极 |
| C.放电过程中NH4+向锌极移动 |
| D.负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
对下列装置的叙述错误的是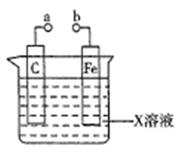
| A.X如果是HCl,则不论a和b用导线连接还是a和b分别连接直流电源正、负极时,H+的移动方向均相同 |
| B.X如果是硫酸铜,a和b分别连接直流电源正、负极,一段时间后铁片质量增加 |
| C.X如果是硫酸铁,则不论a和b是否用导线连接,铁片均发生氧化反应 |
| D.X如果是NaCl,则a和b连接时,该装置可模拟生铁在食盐水中被腐蚀的过程 |
下列物质的有关事实与电化学腐蚀无关的是
| A.轮船水线以下的船壳上镶嵌有一定量的锌块 |
| B.镀锌的铁制品比镀锡的铁制品耐用 |
| C.埋在潮湿疏松土壤里的铁管比干燥致密不透气的土壤里的铁管更易被腐蚀 |
| D.在空气中,金属镁、铝的表面可形成一层氧化膜 |
结合下图判断,下列叙述正确的是
| A.I和Ⅱ中正极均被保护 |
| B.I和Ⅱ中负极反应均是Fe-2e-=Fe2+ |
| C.I和Ⅱ中正极反应均是O2+2H2O+4e-=4OH- |
| D.I和Ⅱ中分别加入少量K3[Fe(CN)6]溶液,均有蓝色沉淀 |
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是
| A.用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl--2e-=Cl2↑ |
| B.氢氧燃料电池的负极反应式:O2+2H2O+4e-=4OH- |
| C.粗铜精炼时,与电源正极相连的是纯铜,阳极反应式为Cu-2e-=Cu2+ |
| D.钢铁发生电化学腐蚀的正极反应式:Fe-2e-=Fe2+ |
下列叙述中,正确的是
①电解池是将化学能转变为电能的装置
②原电池是将电能转变成化学能的装置
③金属和石墨导电均为物理变化,电解质溶液导电伴随化学变化
④不能自发进行的氧化还原反应,通过电解的原理有可能实现
⑤电镀过程相当于金属的“迁移”,可视为物理变化
| A.①②③④ | B.③④ | C.③④⑤ | D.④ |
寒冷的冬天,经常使用暖宝宝,暖宝宝中装的是铁粉、活性炭、无机盐等物质,打开包装以后,可以连续12个小时释放热量,以下分析错误的是
| A.将化学能转化为热能 |
| B.其发热原理与钢铁的吸氧腐蚀相同 |
| C.铁作负极,电极反应为:Fe – 3e → Fe3+ |
| D.活性炭作正极,电极反应为:2H2O + O2 + 4e → 4OH- |
能够使反应Cu+2H2O=Cu(OH)2+H2↑发生的是( )
| A.铜片作原电池的负极,碳棒作原电池的正极,氯化钠作电解质溶液 |
| B.铜锌合金在潮湿的空气中发生电化学腐蚀 |
| C.用铜片作阴、阳电极,电解硫酸钠水溶液 |
| D.用铜片作阴、阳电极,电解硫酸铜水溶液 |