题目内容
(15分)A、B、C、D、E、F六种元素,A、B、C属于第四周期元素且单质均为固体,原子处于基态时A、B原子核外电子均成对,且核电荷数A>B;C与A在周期表属于同一区的元素,如图是金属B和C所形成的某种合金的晶胞结构示意图;D、E、F均位于p区,D原子在基态时p轨道半充满且电负性是同族元素中最大的;E、F的原子均有三个能层,E原子的第一至第四电离能(kj/mol)分别为:578、1817、2745、ll575;E与F能形成原子数目比为1:3、熔点为190℃的化合物Q

(1)写出A的基态核外电子排布式 ;用最简式表示B、C形成合金的组成
(用B、C元素符号表示)。该合金的密度为 a g/cm3,其晶胞的边长为 。
(2)C2+和A2+都能与NH3、H20等形成配位数为4的配合物。[A(NH3)4]2+和[C(NH3)4]2+空间构型不同且都具有对称性,则[C(NH3)4]2+的空间构型为 。[A(NH3)4]2+中A原子轨道的杂化方式为 。
(3) 含有D、碳、硫三种元素的负一价离子中,所有原子均满足最外层8电子结构,一个电子是由硫原子所得,则其电子式为 。
(4)实验测得气态无水Q在1.Ol×105 Pa、t1℃的密度为5.OO g·L-1、气体摩尔体积为53.4 L·mol-,则此时Q的组成为(写化学式) ,
(1)1s22s22p63s23p63d104s2或[Ar]3d104s2
CaCu5 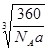 cm(3分) (2)平面正方形
sp3 (3)
cm(3分) (2)平面正方形
sp3 (3)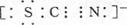 (4)A12C16
(4)A12C16
【解析】根据A、B原子核外电子均成对,且核电荷数A>B,所以A是锌,B是钙。C与A在周期表属于同一区的元素,且二者位于同一周期,所以C是铜。D原子在基态时p轨道半充满且电负性是同族元素中最大的,所以D是氮元素。EF属于第三周期,根据E的电离能可知,E是铝元素。E与F能形成原子数目 比为1:3、熔点为190℃的化合物Q,所以F是氯元素。
(1)根据晶胞的结构图可知,含有的钙原子数是8×1/8=1,铜原子是8×1/2+1=5,所以化学式为CaCu5。设边长为x,则x3×a g/cm3=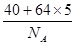 ,解得x=
,解得x=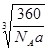 cm。
cm。
(2)[A(NH3)4]2+和[C(NH3)4]2+空间构型不同且都具有对称性,说明[C(NH3)4]2+的空间构型是平面正方形,[A(NH3)4]2+是正四面体型结构,所以是sp3杂化。
(3)所有原子均满足最外层8电子结构,所以氮和碳形成的是三键,因此电子数为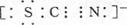 。
。
(4)根据密度和气体的摩尔体积可知,Q的相对分子质量是53.4×5.00=267,所以化学式为A12C16。



 2CA3(g)
2CA3(g)  B
B D
D B转化的化学方程式:
。
B转化的化学方程式:
。