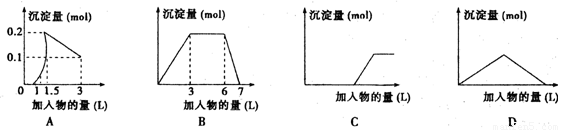题目内容
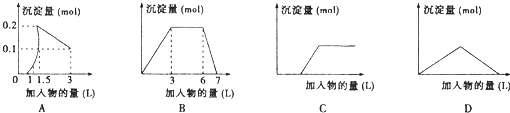
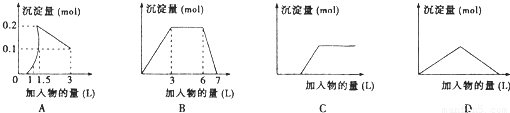
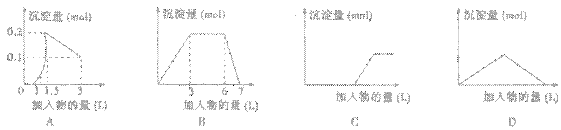
下列曲线图(纵坐标为沉淀的量,横坐标为加入物的量)不正确的是( )
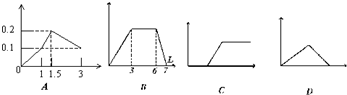

| A、向1L浓度均为0.1mol/L的Ba(OH)2、KAlO2混合液加入0.1mol/L稀H2SO4 | B、向0.1mol/L 明矾和0.3mol/L NH4Cl的混合液1L中加入0.1mol/L NaOH溶液 | C、向硫酸亚铁溶液滴加过量氨水 | D、向Ca(OH)2溶液中逐渐通入二氧化碳 |
分析:A、Ba(OH)2、KAlO2混合液中加入稀H2SO4溶液,酸碱中和反应先发生,然后是硫酸和NaAlO2发生反应的过程;
B、向明矾和NH4Cl的混合液先出现白色沉淀氢氧化铝,然后是铵根离子和氢氧根离子之间反应生成一水合氨,最后是氢氧化铝溶解的过程;
C、向硫酸亚铁溶液滴加过量氨水立即产生白色沉淀;
D、Ca(OH)2溶液中逐渐通入二氧化碳,开始会出现白色沉淀,然后沉淀逐渐消失.
B、向明矾和NH4Cl的混合液先出现白色沉淀氢氧化铝,然后是铵根离子和氢氧根离子之间反应生成一水合氨,最后是氢氧化铝溶解的过程;
C、向硫酸亚铁溶液滴加过量氨水立即产生白色沉淀;
D、Ca(OH)2溶液中逐渐通入二氧化碳,开始会出现白色沉淀,然后沉淀逐渐消失.
解答:解:A、Ba(OH)2、KAlO2混合液中加入稀H2SO4溶液,酸碱中和反应先发生生成硫酸钡沉淀,然后是硫酸和NaAlO2发生反应的过程,当NaAlO2向加入2.5L硫酸,沉淀氢氧化铝全部溶解生成硫酸铝,故A正确;
B、向明矾和NH4Cl的1L混合液中加入NaOH溶液,先出现白色沉淀氢氧化铝,然后是铵根离子和氢氧根离子之间反应生成一水合氨,最后是氢氧化铝溶解的过程,消耗硫酸的量之比是3:3:1,故B正确;
C、向硫酸亚铁溶液滴加过量氨水立即产生白色沉淀,化学方程式为:FeSO4+2NH3?H2O=Fe(OH)2↓+(NH4)2SO4,故C错误;
D、Ca(OH)2溶液中逐渐通入二氧化碳,开始会出现白色沉淀,然后沉淀逐渐消失,两个过程消耗的二氧化碳的量相等,故D正确;
故选:C.
B、向明矾和NH4Cl的1L混合液中加入NaOH溶液,先出现白色沉淀氢氧化铝,然后是铵根离子和氢氧根离子之间反应生成一水合氨,最后是氢氧化铝溶解的过程,消耗硫酸的量之比是3:3:1,故B正确;
C、向硫酸亚铁溶液滴加过量氨水立即产生白色沉淀,化学方程式为:FeSO4+2NH3?H2O=Fe(OH)2↓+(NH4)2SO4,故C错误;
D、Ca(OH)2溶液中逐渐通入二氧化碳,开始会出现白色沉淀,然后沉淀逐渐消失,两个过程消耗的二氧化碳的量相等,故D正确;
故选:C.
点评:本题考查学生物质的性质以及化学反应发生的先后知识,结合图象来考查,增加了题目的难度,平时注意特殊化学反应方程式的积累.

练习册系列答案
相关题目