题目内容
5.已知:2SO2 (g)+O2(g)?2SO3(g)△H<0且压强P1>P2,下列图象中曲线变化正确的是( )| A. |  | B. |  | C. | 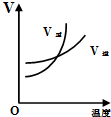 | D. |  |
分析 对于反应2SO2(g)+O2(g)?2SO3(g)△H<0,正反应是体积减小的放热反应,升高温度平衡向逆反应移动,SO3的体积φ(SO3)减小;增大压强平衡向正反应移动,SO3的体积φ(SO3)增大.
解答 解:A、由于该反应是放热反应,升高温度,平移逆向移动,因此SO2的含量增加,与实际图象不符合,故A错误;
B、由于该反应是气体体积减小的反应,温度一定时,增大压强,平衡正向移动,因此P1时SO3的百分含量比P2大,与实际图象符合,故B正确;
C、由于该反应为放热反应,升高温度,正逆反应速率都增大,平衡逆向移动,则逆反应增大幅度比正反应大,与实际图象不符合,故C错误;
D、由于该反应为放热反应,升高温度,平衡逆向移动,K减小,与实际图象不符合,故D错误.
故选:B.
点评 本题主要考查平衡移动图象、外界条件对化学平衡移动的影响等,难度中等,根据图象采取定一议二法分析改变条件与φ(SO3)变化关系是关键.

练习册系列答案
相关题目
15.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,2.24 L CCl4中含有的分子数为0.1NA | |
| B. | 1L 0.1 mol•L-1 NaHCO3溶液中含有0.1NA个HCO3- | |
| C. | 0.1 mo1铁粉在0.1 mol氯气中充分燃烧,失去的电子数目为0.3NA | |
| D. | 1 mol苯含有6 NA个C-H键 |
16.ClO2是一种高效安全的绿色杀菌剂,下列有关ClO2制备与杀菌的说法不合理的是( )
| A. | 可用Cl2和NaClO3制备ClO2,其中n (氧化剂):n (还原剂)=1:2 | |
| B. | ClO2在强碱性环境中使用失效:2ClO2+2OH-═ClO3-+ClO2-+H2O | |
| C. | ClO2处理饮用水时残留的ClO2-,可用FeSO4来除去:ClO2-+2Fe2++4H+═2Fe3++Cl-+2H2O | |
| D. | 等物质的量的ClO2杀菌效果比Cl2、HClO强 |
13.反应mA(s)+nB(g)?pC(g)△H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( )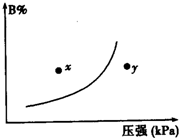
①m+n>p ②y点表示的正反应速率小于逆反应速率
③n>p ④x点比y点时的反应速率慢
⑤若降低温度,该反应的平衡常数增大.

①m+n>p ②y点表示的正反应速率小于逆反应速率
③n>p ④x点比y点时的反应速率慢
⑤若降低温度,该反应的平衡常数增大.
| A. | ①②⑤ | B. | ②④⑤ | C. | 只有①③ | D. | ①③⑤ |
20.已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol 在恒容的密闭容器中充入1molN2和3molH2,一定条件下发生反应,下列说法正确的是( )
| A. | 平衡后,缩小容器的容积,N2的浓度增大 | |
| B. | 平衡后,再向容器中充入1mol氦气,N2的转化率增大 | |
| C. | 平衡前,随着反应的进行,容器内气体密度逐渐增大 | |
| D. | 平衡时,该反应放出的热量为92.4kJ |
17.下列反应是氧化还原反应,且反应的焓变大于零的是( )
| A. | 铝片与稀H2SO4反应 | B. | Ba( OH)2•8H2O与NH4Cl反应 | ||
| C. | 灼热的炭与CO2反应 | D. | 甲烷在O2中的燃烧反应 |
14.A、B、C、D是短周期中原子序数依次增大的元素,其相关信息如下表:
(1)B元素为O(填元素符号),B单质与Na剧烈反应生成的化合物中的化学键类型是离子键、共价键.
(2)C元素的单质与水反应可产生使带余烬的木条复燃的气体,该反应的化学方程式为2F2+2H2O=4HF+O2.
(3)由A、D两种元素组成的-种化合物X分子中,所有原子的最外层均达到8电子稳定结构,则X的电子式为 .X常用作漂白剂,也用于柠檬等水果的熏蒸处理.已知化合物X中,A显负价,D显正价,则该化合物与水反应的化学方程式为NCl3+4H2O=NH3.H2O+3HClO.
.X常用作漂白剂,也用于柠檬等水果的熏蒸处理.已知化合物X中,A显负价,D显正价,则该化合物与水反应的化学方程式为NCl3+4H2O=NH3.H2O+3HClO.
| 元素 | 相关信息 |
| A | 简单氢化物能与其最高价含氧酸反应生成盐 |
| B | 原子最外层电子数是其电子层数的3倍 |
| C | 周期表中非金属性最强的元素 |
| D | 与C位于同主族,且都为短周期元素 |
(2)C元素的单质与水反应可产生使带余烬的木条复燃的气体,该反应的化学方程式为2F2+2H2O=4HF+O2.
(3)由A、D两种元素组成的-种化合物X分子中,所有原子的最外层均达到8电子稳定结构,则X的电子式为
 .X常用作漂白剂,也用于柠檬等水果的熏蒸处理.已知化合物X中,A显负价,D显正价,则该化合物与水反应的化学方程式为NCl3+4H2O=NH3.H2O+3HClO.
.X常用作漂白剂,也用于柠檬等水果的熏蒸处理.已知化合物X中,A显负价,D显正价,则该化合物与水反应的化学方程式为NCl3+4H2O=NH3.H2O+3HClO.  为将CO和NO转化为无毒物质,某同学设计了如图装置.
为将CO和NO转化为无毒物质,某同学设计了如图装置.