题目内容
能在水溶液中大量共存的一组离子是( )
| A.H+、Fe3+、I-、SO42- | B.Al3+、Mg2+、HCO3-、Cl- |
| C.K+、Ag+、Ca2+、PO43- | D.NH4+、Na+、SO42-、Cl- |
D
解析试题分析:Fe3+ 具有较强氧化性不能与还原性强的I- 共存,A错误;Al3+与HCO3-易发生双水解,B错误;Ag+、Ca2+与PO43- 均能生成难溶的沉淀而不能大量共存,C错误;D中离子可以共存,选D。
考点:本题考查的是

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列化学反应式书写正确的是
A.制取氢氧化铁胶体的化学方程式为FeCl3+3H2O Fe(OH)3(胶体)+3HCl Fe(OH)3(胶体)+3HCl |
B.亚硫酸在溶液中的电离方程式为H2SO 2H++SO32- 2H++SO32- |
C.NaHCO3水解的离子方程式为HCO3-+H2O CO32-+H3O+ CO32-+H3O+ |
| D.电子工业印刷电路反应式为2Fe3++Cu=Cu2++2Fe2+ |
下列各组离子可能大量共存的是
| A.能使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、S2-、Br- |
| B.遇pH试纸变红色的溶液:Fe2+、S2O32-、SO42-、Na+ |
| C.水电离出的c(H+) ?c(OH-) =10-28的溶液:Na+、S2-、NO3-、SO32- |
| D.能使KSCN显红色的溶液:Na+、NH4+、AlO2-、CO32- |
下列反应的离子方程式正确的是
A.铝片跟氢氧化钠溶液反应:Al+2OH-=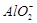 +H2↑ +H2↑ |
B.硫酸镁溶液跟氢氧化钡溶液反应: +Ba2+=BaSO4↓ +Ba2+=BaSO4↓ |
| C.碳酸钙跟醋酸反应:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ |
D.铜片跟稀硝酸反应:Cu+ +4H+=Cu2++NO↑+2H2O +4H+=Cu2++NO↑+2H2O |
下列离子方程式正确的是( )
| A.Cl2通入水中:Cl2 + H2O = 2H+ + Cl— + ClO— |
| B.双氧水中加入稀硫酸和KI溶液:H2O2 + 2H+ + 2I— = I2 + 2H2O |
C.用铜作电极电解CuSO4溶液:2Cu2+ + 2H2O  2Cu + O2↑+ 4H+ 2Cu + O2↑+ 4H+ |
| D.Na2S2O3溶液中加入稀硫酸:2S2O32—+4H+ = SO42— + 3S↓ + 2H2O |
某无色溶液中可能含有①Na+ ②Ba2+ ③Cl- ④Br- ⑤SO32- ⑥SO42-中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
| 步骤序号 | 操 作 步 骤 | 现 象 |
| (1) | 用pH试纸检验 | 溶液的pH>7 |
| (2) | 向溶液中滴加氯水,再加入CCl4、振荡、静置 | 下层呈橙色 |
| (3) | 向(2)所得水溶液加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀产生 |
| (4) | 过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
下列结论正确的是:
A.不能确定的离子是① B.不能确定的离子是③⑥
C.肯定没有的离子是②⑤ D.肯定含有的离子只有④⑤
下列各组离子在指定溶液中能大量共存的是( )。
| A.无色溶液中:K+、Na+、MnO4-、SO42- |
| B.酸性溶液中:Fe2+、Al3+、NO3-、I-、Cl- |
| C.加入Al能放出H2的溶液中:HCO3-、NO3-、Mg2+、Na+ |
| D.pH=11的溶液中:CO32-、Na+、AlO2-、NO3- |
下列微粒能够大量共存的是( )
| A.在pH=14的溶液中:HCO3-、Cl-、SO32-、K+ |
| B.在无色透明溶液中:Cu2+、K+、SO42-、Cl一 |
| C.在苯酚溶液中:Br-、Fe3+、NO3-、Cl- |
| D.在新制Cu(OH)2悬浊液中: CH3CHO、C2H5OH、SO42-、Na+ |
下列示意图与对应的反应情况符合的是( )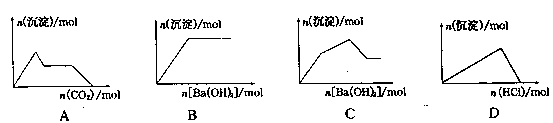
| A.向含0.01mol KOH和0.01mol Ca(OH)2的混合溶液中缓慢通入CO2至过量 |
| B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量 |
| C.向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至过量 |
| D.向NaAlO2溶液中逐滴加入盐酸至过量 |