题目内容
下列表述中正确的是
A 任何能使熵值增大的过程都能自发进行
B △H<0,△S>0的化学反应一定能自发进行
C 已知热化学方程式2SO2(g)+O2(g)
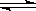 2SO3(g);△H=-QkJ·mol-1(Q>0),
2SO3(g);△H=-QkJ·mol-1(Q>0),
则将2mol SO2(g) 和1mol O2(g) 置于一密闭容器中充分反应后放出Q kJ的热量
D 稀溶液中1mol NaOH分别和1mol CH3COOH、1molHNO3反应,两者放出的热量一样多
【答案】
B
【解析】根据△G=△H-T△S可知,当△G小于0时,反应才是自发进行的所以A不正确,B正确。C不正确,可逆反应的转化率不可能是100%的。醋酸是弱电解质,大量要吸热,所以醋酸和氢氧化钠反应放出热量要小于硝酸和氢氧化钠反应放出的热量。答案选B。

练习册系列答案
相关题目
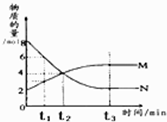 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为:N?2M | B、t2时,反应不再发生 | C、t2时,正反应速率等于逆反应速率 | D、t3后,反应到达最大限度 |
 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )