题目内容
下列表述中正确的是( )
分析:A.电解质的强弱是根据其电离程度划分的,完全电离的是强电解质;
B.多元弱酸根的水解是分步水解的;
C.多元弱酸是分步电离的;
D.氯化铁是强酸弱碱盐,溶于水能水解,为防止变质,应加入酸抑制其水解.
B.多元弱酸根的水解是分步水解的;
C.多元弱酸是分步电离的;
D.氯化铁是强酸弱碱盐,溶于水能水解,为防止变质,应加入酸抑制其水解.
解答:解:A.氯化铵溶于水完全电离,所以氯化铵是强电解质,但因为铵根离子水解而导致其溶液呈酸性,故A错误;
B.纯碱溶液的水解方程式为CO32-+H2O?HCO3-+OH-,故B错误;
C.碳酸是二元弱酸,其电离方程式为:H2CO3?H++HCO3-,故C错误;
D.氯化铁是强酸弱碱盐,溶于水能水解而使其溶液呈酸性,为防止其水解,应先将FeCl3溶于较浓的盐酸中,然后再加水稀释到所需浓度,故D正确;
故选D.
B.纯碱溶液的水解方程式为CO32-+H2O?HCO3-+OH-,故B错误;
C.碳酸是二元弱酸,其电离方程式为:H2CO3?H++HCO3-,故C错误;
D.氯化铁是强酸弱碱盐,溶于水能水解而使其溶液呈酸性,为防止其水解,应先将FeCl3溶于较浓的盐酸中,然后再加水稀释到所需浓度,故D正确;
故选D.
点评:本题考查强弱电解质的判断、水解方程式、电离方程式的书写等知识点,注意书写水解方程式和弱电解质的电离方程式时要写可逆号,不能写等号,为易错点.

练习册系列答案
相关题目
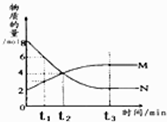 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为:N?2M | B、t2时,反应不再发生 | C、t2时,正反应速率等于逆反应速率 | D、t3后,反应到达最大限度 |
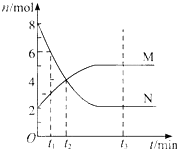 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )