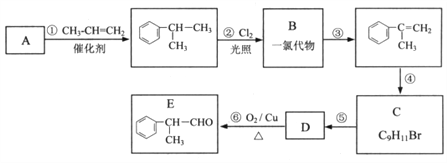
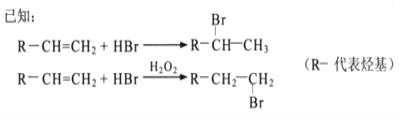
题目内容
【题目】锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231℃;Sn2+易水解、易被氧化。请按要求回答下列相关问题:
(1)SnSO4可使酸性KMnO4溶液褪色,该过程中Sn2+转化为Sn4+,该反应的离子方程式为_______。
(2)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:

①步骤Ⅰ加入Sn粉的作用: _______________________。
②步骤Ⅱ用到的玻璃仪器有烧杯、_____________________________。
③步骤Ⅲ生成SnO的离子方程式:_________________________。
④步骤Ⅳ中检验SnO是否洗涤干净的操作是____________________,证明已洗净。
⑤步骤Ⅴ由SnSO4溶液得到SnSO4晶体的操作依次为 ________ 、 ________、过滤、洗涤、低温干燥。
【答案】 5Sn2++2MnO4-+16H+=5Sn4++2Mn2++8H2O 防止Sn2+被氧化为Sn4+ 漏斗、玻璃棒 Sn2++2HCO3-==SnO↓+2CO2↑+H2O 取最后一次洗涤液少许于试管中,加入足量的HNO3酸化的AgNO3溶液,若无白色沉淀,则已洗净,反之则没有洗净 蒸发浓缩 冷却结晶
【解析】(1)、SnSO4可使酸性KMnO4溶液褪色,该过程中Sn2+转化为Sn4+,说明KMnO4作氧化剂,生成Mn2+,故其反应的离子方程式是:5Sn2++2MnO4-+16H+=5Sn4++2Mn2++8H2O。
(2)、①.由于Sn2+易水解、易被氧化,加入盐酸,抑制Sn2+水解,加入Sn粉可以与盐酸反应,调节溶液pH,还可以防止Sn2+被氧化为Sn4+,故答案是:防止Sn2+被氧化为Sn4+。
②.步骤Ⅱ为过滤,过滤需要用到的玻璃仪器是烧杯、漏斗、玻璃棒,故答案是:漏斗、玻璃棒。
③. 得到沉淀是SnO,Sn元素化合价未发生变化,属于非氧化还原反应,变质发生水解反应生成Sn(OH)2与二氧化碳,Sn(OH)2再脱水得到SnO,反应离子方程为:Sn2++2HCO3=SnO↓+2CO2↑+H2O,故答案为:Sn2++2HCO3=SnO↓+2CO2↑+H2O;
④. 沉淀为SnO,表面附着有Cl,要想检验滤渣是否洗涤干净,可以用硝酸、硝酸银溶液检验最后一次洗涤液中是否含有Cl,具体方案为:取最后一次滤液少许于试管中,依次滴加足量硝酸酸化的硝酸银溶液,观察到无白色沉淀,说明洗涤干净,反之则没有洗净。
故答案为:取最后一次洗涤液少许于试管中,加入足量的HNO3酸化的AgNO3溶液,若无白色沉淀,则已洗净,反之则没有洗净。
⑤.由流程图可知,操作V是由SnSO4溶液得到SnSO4晶体,只能采取蒸发浓缩、冷却结晶、过滤、洗涤得到,故答案为:蒸发浓缩、冷却结晶。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案【题目】在Na+浓度为0.5molL﹣1的某澄清溶液中,还可能含有下表中的若干种离子:
阳离子 | K+、Ag+、Mg2+ |
阴离子 | NO3﹣、CO32﹣、SiO32﹣、SO42﹣ |
取该溶液100mL进行如下实验(气体体积在标准状况下测定):
序号 | 实验内容 | 实验结果 |
Ⅰ | 向该溶液中加入足量稀HCl | 产生白色沉淀并放出0.56L气体 |
Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4g |
Ⅲ | 在Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
试回答下列问题:
(1)实验Ⅰ能确定一定不存在的离子是 .
(2)实验Ⅰ中生成沉淀的离子方程式为 .
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,填写下表中阴离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)
阴离子 | NO3﹣ | CO32﹣ | SiO32﹣ | SO42﹣ |
c/molL﹣1 |
(4)判断原溶液中K+是否存在,若存在,求其最小物质的量浓度,若不存在,请说明理由: .