题目内容
【题目】煤燃烧排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝完成下列填空:
(1)上述烟气处理过程中涉及到的化学物质,其组成元素中属于第三周期元素的是______;写出N的核外电子排布式______。
(2)已知SO2分子的空间构型折线形,则SO2为______(选填“极性”、“非极性”)。
(3)将含有SO2和NOx的烟气通入盛有NaClO2溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如下(其他离子忽略不计):
离子 | Na+ | SO42- | NO3- | OH- | Cl- |
浓度/(molL-1) | 5.5×10-3 | 8.5×10-4 | y | 2.0×10-4 | 3.4×10-3 |
①表中y=______molL-1。
②写出NaClO2溶液吸收SO2的离子方程式______。
(4)烟气中的SO2还可采用氨法脱硫除去,其反应原理可用如图表示。
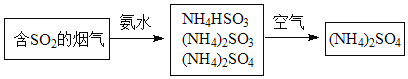
①写出SO2跟氨水反应生成NH4HSO3的化学方程式______。
②(NH4)2HSO3溶液中浓度最大的离子是______。
【答案】S、Na、Cl 1s22s22p3 极性 2.0×10-4 2SO2+ClO-+2H2O=2SO4+Cl-+4H+ SO2+NH3H2O=NH4HSO3 NH4+
【解析】
(1)硫、钠、氯为第三周期元素,N原子的核外有两个能级,第2个能层上有s、p能级;
(2)SO2分子为空间构型为结构不对称的折线形;
(3)①溶液呈电中性,依据电荷守恒关系计算;
②二氧化硫和NaClO2溶液发生氧化还原反应生成硫酸和氯化钠;
(4)①二氧化硫是酸性氧化物和一水合氨反应生成亚硫酸氢铵;
(1)煤燃烧排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝反应,其组成元素中属于第三周期元素为硫、钠、氯,N原子的核外有两个能层,第2个能层上有s、p能级,N原子电子排布式为1s22s22p3, 故答案为:S、Na、Cl;1s22s22p3;
(2)SO2分子的空间构型折线形,分子中正负电荷中心不重合,SO2为极性分子,故答案为:极性;
(3)①溶液呈电中性,溶液中存在电荷守恒关系c(Na+)=c(Cl-)+c(OH-)+c2c(SO42-)+y,则表中的y=5.5×10-3-3.4×10-3-2.0×10-4-2×8.5×10-4=5.8×10-4,y=2.0×10-4,故答案为:2.0×10-4;
②二氧化硫和NaClO2溶液发生氧化还原反应生成硫酸和氯化钠,反应的离子方程式为2SO2+ClO2-+2H2O=2SO42-+Cl-+4H+,故答案为:2SO2+ClO-+2H2O=2SO4+Cl-+4H+;
(4)①二氧化硫是酸性氧化物,其和一水合氨反应生成亚硫酸氢铵,反应的化学方程式为SO2+NH3H2O=NH4HSO3,故答案为:SO2+NH3H2O=NH4HSO3;
②(NH4)2HSO3是强电解质,在溶液中完全电离出铵根离子和亚硫酸氢根离子,亚硫酸氢根离子的电离大于铵根离子的水解,溶液呈酸性,则浓度最大的离子是NH4+,故答案为:NH4+。

 华东师大版一课一练系列答案
华东师大版一课一练系列答案