题目内容
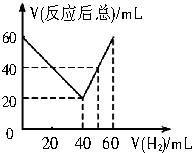
【题目】室温条件下在醋酸和醋酸钠的混合溶液中,当c(CH3COOH)+c(CH3COO﹣)=0.lmolL﹣1时,c(CH3COOH)、c(CH3COO﹣)与pH的关系如图所示.下列有关叙述正确的是( )
A.W点所表示的溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH﹣)
B.pH=5.5的溶液中:c(CH3COOH)>c(CH3COO﹣)>c(H+)>c(OH﹣)
C.pH=3.5的溶液中:c(Na+)+c(H+)+c(OH﹣)+c(CH3COOH)=0.1mol.L﹣l
D.表示CH3COO﹣浓度变化的是曲线Ⅰ
【答案】B
【解析】解:A.W点为等量的醋酸和醋酸钠的混合液,W点由电荷守恒可知,c(Na+)+c(H+)=c(CH3COO﹣)+c(OH﹣),故A错误;
B.由图可知,pH=5.5 的溶液,显酸性,且c(CH3COO﹣)<c(CH3COOH),显性离子大于隐性离子,则c(CH3COOH)>c(CH3COO﹣)>c(H+)>c(OH﹣),故B正确;
C.由电荷守恒及c(CH3COOH)+c(CH3COO﹣)=0.1molL﹣1可知,c(Na+)+c(H+)﹣c(OH﹣)+c(CH3COOH)=c(CH3COO﹣)+c(OH﹣)﹣c(OH﹣)+c(CH3COOH)=0.1mol/L,故C错误;
D.随溶液PH越大,醋酸根离子浓度越大,表示CH3COO﹣浓度变化的是曲线Ⅱ,故D错误;
故选B.
【考点精析】根据题目的已知条件,利用弱电解质在水溶液中的电离平衡的相关知识可以得到问题的答案,需要掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.

 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案