题目内容
海洋是个巨大的资源宝库,海水资源的利用具有非常广阔的发展前景。海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下所示:
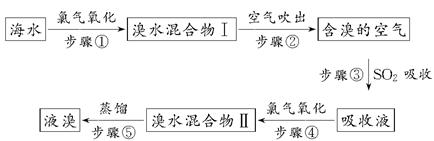
(1)步骤①反应的廊子方程式为_______________________________。
(2)步骤③反应的化学方程式为_________________________________。
(3)Br的原子序数是________,在周期表中位于第________周期、________族。
(4)步骤⑤蒸馏的过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因:________________。
(5)为什么不直接用“溴水混合物Ⅰ”而要用“溴水混合物Ⅱ”进行蒸馏,得出液溴?

(1)步骤①反应的廊子方程式为_______________________________。
(2)步骤③反应的化学方程式为_________________________________。
(3)Br的原子序数是________,在周期表中位于第________周期、________族。
(4)步骤⑤蒸馏的过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因:________________。
(5)为什么不直接用“溴水混合物Ⅰ”而要用“溴水混合物Ⅱ”进行蒸馏,得出液溴?
(1)2Br-+Cl2=Br2+2Cl- (2)SO2+Br2+2H2O=2HBr+H2SO4 (3)35 四 ⅦA (4)温度过高,大量水蒸气随溴蒸气排出,溴蒸气中水增加,温度过低,溴不能完全蒸出,回收率降低 (5)“溴水混合物Ⅰ”中虽然含有溴单质,但浓度低,如果直接蒸馏,处理量大,生产成本高;经过“空气吹出、SO2吸收、氯气氧化”等步骤实际上是将溴水浓缩了
(1)Cl的非金属性大于Br,海水中含有的Br-被氯气置换,Cl2+2Br-=Br2+2Cl-。
(2)空气中的Br2与SO2反应,得到含高浓度Br-的溶液,SO2+2H2O+Br2=2HBr+H2SO4。
(3)溴为第四周期,ⅦA族元素;根据各周期元素的个数,计算第四周期稀有气体元素的原子序数,由此推出Br的原子序数=2+8+8+18-1=35。
(4)根据蒸馏分离原理进行回答。水的沸点为100℃,温度过高水蒸发量增大,温度过低,溴的挥发量减少,不能完全蒸出,回收率降低。
(5)海水中Br-的含量很低,因此“溴水混合物Ⅰ”中溴的含量很低,直接蒸馏,处理液体的量很大,能耗高,成本增加;经过一系列处理后的“溴水混合物Ⅱ”中Br2的浓度增大,蒸馏时,所需处理的液体量大大减少,能耗降低,成本降低。
(2)空气中的Br2与SO2反应,得到含高浓度Br-的溶液,SO2+2H2O+Br2=2HBr+H2SO4。
(3)溴为第四周期,ⅦA族元素;根据各周期元素的个数,计算第四周期稀有气体元素的原子序数,由此推出Br的原子序数=2+8+8+18-1=35。
(4)根据蒸馏分离原理进行回答。水的沸点为100℃,温度过高水蒸发量增大,温度过低,溴的挥发量减少,不能完全蒸出,回收率降低。
(5)海水中Br-的含量很低,因此“溴水混合物Ⅰ”中溴的含量很低,直接蒸馏,处理液体的量很大,能耗高,成本增加;经过一系列处理后的“溴水混合物Ⅱ”中Br2的浓度增大,蒸馏时,所需处理的液体量大大减少,能耗降低,成本降低。

练习册系列答案
相关题目