题目内容
短周期元素E的氯化物ECln的熔点为-78℃,沸点为59℃;若0.2molECln与足量的AgNO3溶液完全反应后可以得到57.4g的AgCl沉淀。下列判断错误的是
| A.E可能是一种金属元素 |
| B.在ECln中E与Cl之间形成共价键 |
| C.E位于元素周期表的IVA族 |
| D.E的一种氧化物为EO |
C
试题分析:57.4g的AgCl的物质的量是0.4mol,0.2molECln与足量的AgNO3溶液完全反应后生成0.4molAgCl,说明ECln中n=2。A、E可能为+2价金属,正确;B、ECln的熔点为-78℃,沸点为59℃比较低,根据晶体类型的熔沸点高低的判断,ECln应为分子晶体,E与Cl之间形成共价键,正确;C、元素周期表的IVA族元素的化合价一般为+4价,短周期内只有CO中C为+2价,所以E不是IVA族元素,错误;D、E的化合价为+2,所以氧化物化学式为EO,正确,答案选C。

练习册系列答案
相关题目
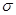 ”或“
”或“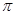 ”)。
”)。