题目内容
元素周期表前四周期A、B、C、D、E五种元素,A元素的原子最外层电子排布式为ms1;B元素的原子价电子排布式为ns2np2;C元素位于第二周期且原子中p能级与s能级电子总数相等;D元素原子的M能层的p能级中有3个未成对电子;E元素原子有五个未成对电子。
(1)写出元素名称:C 、D 、E 。
(2)C基态原子的电子排布图为___________________,若A为非金属元素,则按原子轨道的重叠方式,A与C形成的化合物中的共价键属于________键(填“σ”或“π”)。
(3)当n=2时,B的最简单气态氢化物的电子式为____________,BC2分子的结构式是 ______________;当n=3时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是 。 (4)若A元素的原子最外层电子排布为2s1,B元素的原子价电子排布为3s23p2,A、B、C、D四种元素的第一电离能由大到小的顺序是__________________(用元素符号表示)。
(5)E元素原子的特征电子构型是 ,在元素周期表中位置是 ,其最高价氧化物的化学式是 。
(1)写出元素名称:C 、D 、E 。
(2)C基态原子的电子排布图为___________________,若A为非金属元素,则按原子轨道的重叠方式,A与C形成的化合物中的共价键属于________键(填“σ”或“π”)。
(3)当n=2时,B的最简单气态氢化物的电子式为____________,BC2分子的结构式是 ______________;当n=3时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是 。 (4)若A元素的原子最外层电子排布为2s1,B元素的原子价电子排布为3s23p2,A、B、C、D四种元素的第一电离能由大到小的顺序是__________________(用元素符号表示)。
(5)E元素原子的特征电子构型是 ,在元素周期表中位置是 ,其最高价氧化物的化学式是 。
(1)氧 磷 锰 (2)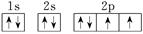 σ键
σ键
(3)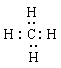 ;O=C=O SiO2 + 2OH-=SiO32- +H2O(2分)
;O=C=O SiO2 + 2OH-=SiO32- +H2O(2分)
(4)O>P>Si>Li
(5)3d54s2 第四周期 ⅦB族 Mn2O7
 σ键
σ键(3)
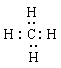 ;O=C=O SiO2 + 2OH-=SiO32- +H2O(2分)
;O=C=O SiO2 + 2OH-=SiO32- +H2O(2分)(4)O>P>Si>Li
(5)3d54s2 第四周期 ⅦB族 Mn2O7
试题分析:A元素的原子最外层电子排布式为ms1,则A是第IA族元素;B元素的原子价电子排布式为ns2np2,所以B应该是第ⅣA族元素;C元素位于第二周期且原子中p能级与s能级电子总数相等,所以C是氧元素;D元素原子的M能层的p能级中有3个未成对电子,则D是P元素;E元素原子有五个未成对电子,则E的原子序数是25,属于第四周期的Mn元素。
(1)C、D、E的元素名称是氧、磷、锰。
(2)氧元素的核电荷数是8,则根据构造原理、能量最低原理、洪特规则以及泡利原理可知,其轨道表达式为
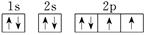 。A为非金属元素,因此A是氢元素。则按原子轨道的重叠方式,H与O形成的化合物中的共价键属于头碰头重叠,即为σ键。
。A为非金属元素,因此A是氢元素。则按原子轨道的重叠方式,H与O形成的化合物中的共价键属于头碰头重叠,即为σ键。(3))当n=2时,B是碳元素,其最简单气态氢化物是甲烷,含有极性键的非极性分子,电子式为
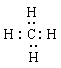 ;BC2分子是CO2,属于直线型结构,其结构式是O=C=O;当n=3时,B是Si元素。B与C形成的化合物二氧化硅与氢氧化钠溶液反应的离子方程式是SiO2 + 2OH-=SiO32- +H2O。
;BC2分子是CO2,属于直线型结构,其结构式是O=C=O;当n=3时,B是Si元素。B与C形成的化合物二氧化硅与氢氧化钠溶液反应的离子方程式是SiO2 + 2OH-=SiO32- +H2O。(4)若A元素的原子最外层电子排布为2s1,则A是Li。B元素的原子价电子排布为3s23p2,则B是Si元素。由于非金属性越强,第一电离能越大,所以氧元素的第一电离能最大。Li是金属第一电离能最小。P的非金属性强于Si,第一电离能大于硅的,所以A、B、C、D四种元素的第一电离能由大到小的顺序是O>P>Si>Li。
(5)E元素是Mn,原子序数是25,位于周期表的第四周期第ⅦB族,所以原子的特征电子构型是3d54s2; 最高价是+7价,因此其最高价氧化物的化学式是Mn2O7。

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案
相关题目
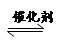 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。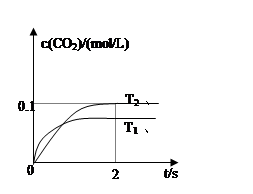
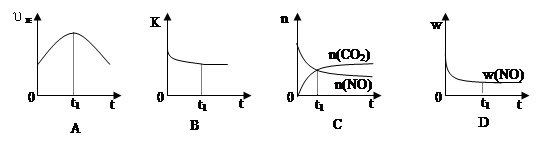
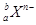 ,下列说法正确的是
,下列说法正确的是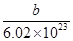 g
g