题目内容
【题目】磷化氢气体(PH3)是一种强烈的储粮害虫杀剂,其制取原理类似于实验室制氨气,空气中磷化氢气体达到2PPM以上是就会造成人畜中毒..,请回答:
(1)用碘化磷(PH4I)和烧碱反应制取PH3的化学方程式______。
(2)实验室用硫酸铜溶液吸收PH3时的化学方程式24CuSO4+11PH3+12H2O=8Cu3P↓+3H3PO4+24H2SO4 中氧化剂是______,当吸收2.2molPH3转移电子______mol
(3)氧硫化碳(COS)可替代磷化氢而被用作熏蒸剂.粉末状的KSCN与浓硫酸在一定条件下可得到COS和两种硫酸氢盐,生成物的物质的量之比为1∶1∶1,写出相应的化学方程式______。
(4)氧硫化碳水解及部分应用流程如下(部分产物已略去):
COS![]() H2S
H2S![]() Na2S
Na2S![]() M溶液+H2
M溶液+H2
①组成氧硫化碳和磷化氢的各原子中,原子半径最大的元素在周期表中的位置是_______.
②已知M溶液中硫元素的主要存在形式为S2O32﹣,则反应Ⅲ中生成S2O32﹣的离子方程式为___.
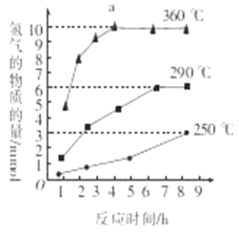
③如图是反应Ⅲ中,在不同反应温度下,反应时间与H2产量的关系(Na2S初始含量为3mmol).由图象分析可知,a点时M溶液中除S2O32﹣外,还有____(填含硫微粒的离子符号).
【答案】 PH4I+NaOH==PH3↑+NaI+H2O CuSO4 4.8 KSCN+2H2SO4(浓)+H2O=KHSO4+NH4HSO4+COS↑ 第三周期第VA族 2S2﹣+5H2O![]() S2O32﹣+4H2↑+2OH﹣ SO42﹣
S2O32﹣+4H2↑+2OH﹣ SO42﹣
【解析】试题分析:(1)根据实验室制取氨气的反应原理可知用碘化磷(PH4I)和烧碱反应制取PH3的化学方程式为PH4I+NaOH![]() PH3↑+NaI+H2O。
PH3↑+NaI+H2O。
(2)根据方程式可知铜元素的化合价从+2价降低到+1价,因此硫酸铜是氧化剂。每消耗24mol硫酸铜,转移24mol电子,所以当吸收2.2molPH3时转移电子的物质的量为![]() 。
。
(3)粉末状的KSCN与浓硫酸在一定条件下可得到COS和两种硫酸氢盐,生成物的物质的量之比为1∶1∶1,根据原子守恒可知两种硫酸氢盐应该是硫酸氢钾和硫酸氢铵。则反应的化学方程式为KSCN+2H2SO4(浓)+H2O=KHSO4+NH4HSO4+COS↑。
(4)①组成氧硫化碳和磷化氢的各原子中,原子半径最大的元素是P,在周期表中的位置是第三周期第VA族。
②已知M溶液中硫元素的主要存在形式为S2O32﹣,则根据流程图可知反应物是硫化钠和水,生成物有硫代硫酸钠、氢气,根据原子守恒可知还应该有氢氧化钠生成,则反应Ⅲ中生成S2O32﹣的离子方程式为2S2﹣+5H2O![]() S2O32﹣+4H2↑+2OH﹣。
S2O32﹣+4H2↑+2OH﹣。
③根据图像可知a点时氢气是10mol,说明反应中有20mol电子转移,则根据电子得失守恒可知3mol硫化钠必须提供20mol电子,全部转化为硫代硫酸钠转移12mol电子,全部转化亚硫酸钠转移18mol电子,全部转化为硫酸钠转移24mol电子,所以a点时M溶液中除S2O32﹣外,还有SO42﹣。

【题目】已知Fe2O3(s)+3CO(g)2Fe(s)+3CO2(g)在不同温度下的平衡常数如表:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 42.9 | 50.7 | 64.0 |
请回答下列问题:
(1)该反应的平衡常数表达式K= ______ ,△H ______ 0(填“>”、“<”或“=”)。
(2)在一个容积为10L的密闭容器中,1300℃时加入Fe、Fe2O3、CO、CO2各1mol,反应经过10min后达到平衡.求该时间范围内反应的平均反应速率v(CO2)= ______ ,CO的平衡转化率为 ______。
(3)欲提高(2)中CO的平衡转化率,可采取的措施是 ______。
A.增加Fe2O3的量B.加入合适的催化剂C.移出部分CO2D.提高反应温度.