题目内容
19.实验室欲用Na2CO3固体配制0.2mol•L-1的Na2CO3溶液100mL:(1)配制溶液时,一般可以分为以下八个步骤:
①计算②称量③溶解 ④定容⑤转移 ⑥洗涤 ⑦冷却 ⑧倒转摇匀
其中④至⑦步骤顺序可能不对,写出由先到后的顺序为⑦⑤⑥④.
(2)完成本实验必须用到的玻璃仪器有烧杯、玻璃杯、100mL容量瓶、胶头滴管.
(3)配制该溶液需用托盘天平准确称取Na2CO3固体2.1g.
(4)使用容量瓶前必须进行的一步操作是检查容量瓶是否漏水.
(5)在配制过程中,如果其他操作都是正确的,下列操作会引起浓度偏高的是④.
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量溶液洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线.
分析 (1)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶来对操作顺序进行排序;
(2)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;
(3)根据n=cV和m=nM来计算;
(4)容量瓶使用前必须查漏;
(5)根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析.
解答 解:(1)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶可知正确的操作顺序是⑦⑤⑥④,故答案为:⑦⑤⑥④;
(2)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶可知所需的仪器有托盘天平、烧杯、玻璃杯、100mL容量瓶、胶头滴管,故还缺少的玻璃仪器有:100mL容量瓶、胶头滴管,故答案为:100mL容量瓶、胶头滴管;
(3)所需的碳酸钠的物质的量n=cV=0.2mol/L×0.1L=0.02mol,质量m=nM=0.02mol×106g/mol=2.1g,故答案为:2.1g;
(4)容量瓶使用前必须查漏,故答案为:检查容量瓶是否漏水;
(5)①没有洗涤烧杯和玻璃棒,会导致溶质的损失,则浓度偏低,故错误;
②转移溶液时不慎有少量溶液洒到容量瓶外面,会导致溶质的损失,则浓度偏低,故错误;
③容量瓶不干燥,含有少量蒸馏水,对浓度无影响,故错误;
④定容时俯视刻度线,则溶液体积偏小,浓度偏高,故正确;
⑤定容摇匀后发现溶液体积低于刻度线是正常的,再补加少量蒸馏水至刻度线,则浓度偏低故错误.
故答案为:④.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.下列有关物质的分类或归类中正确的是( )
| A. | 化合物:HT、CaCl2、NaOH、盐酸 | |
| B. | 纯净物:水玻璃、胆矾晶体、液氯、硫酸 | |
| C. | 天然高分子化合物:淀粉、纤维素、蛋白质、聚氯乙烯 | |
| D. | 同分异构体:CH3CH2CH2CH2CH3、CH3CH2CH(CH3)2、C(CH3)4 |
14.下列化学事实,能用勒夏特列原理解释的是( )
| A. | 对于可逆反应:H2(g)+Br2(g)?2HBr(g)达到化学平衡后,增大压强时,混合气体颜色变深 | |
| B. | 合成氨工业中温度选择为500°C | |
| C. | 配制Al2(SO4)3溶液时加入少量稀硫酸 | |
| D. | 合成氨工业采用循环操作,可提高原料利用率 |
4.化学反应N2(g)+3H2(g)═2NH3(l)的能量变化如图所示,则该反应的△H等于( )


| A. | +2(b-a) kJ•mol-1 | B. | +(b+c-a) kJ•mol-1 | ||
| C. | +(a+b) kJ•mol-1 | D. | +2(a-b-c) kJ•mol-1 |
8.设NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下22.4L水所含的分子为NA | |
| B. | 16g氧气中所含的电子数为NA | |
| C. | 18g水所含的电子数为8NA | |
| D. | NA个Cl2的质量是71g |
9.设NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,11.2 L氧气所含的氧原子数为NA | |
| B. | 1 mol/L的CaCl2溶液中含有的Cl-为2 NA | |
| C. | 2.4 g镁变成Mg2+时失去的电子数目为0.2 NA | |
| D. | 标准状况下,2 g氢气所含的原子数目为NA |

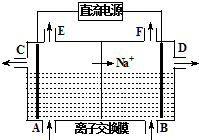 电解原理在工业生产中有广泛的应用.
电解原理在工业生产中有广泛的应用.