题目内容
【题目】液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料 的电池装置如图所示,该电池以空气中的氧气为氧化剂,以 KOH 溶液为电解质溶液.下列 关于该电池的叙述错误的是( ) 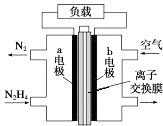
A.b 极发生还原反应
B.a 极的反应式为 N2H4﹣4e﹣═N2↑+4H+
C.放电时,电流从 b 极经过负载流向 a 极
D.其中的离子交换膜需选用阴离子交换膜
【答案】B
【解析】解:A.该燃料电池中,通入氧化剂空气的电极b为正极,正极上氧气得电子发生还原反应,故A正确;
B.通入燃料的电极为负极,负极上燃料失电子发生氧化反应,在碱性条件下,电极反应式为N2H4+4OH﹣﹣4e﹣=N2↑+4H2O,故B错误;
C.放电时,电流从正极b经过负载流向a极,故C正确;
D.该原电池中,正极上生成氢氧根离子,所以离子交换膜要选取阴离子交换膜,故D正确;
故选B.

练习册系列答案
相关题目