题目内容
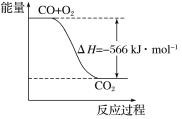
【题目】Ⅰ.工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+2CO2(g)![]() CH3OCH3(g)+3H2O(g)ΔH<0。温度升高,该化学平衡移动后到达新的平衡,CH3OCH3的产率将________(填“变大”、“变小”或“不变”,下同),混合气体的平均相对分子质量将_____________________。
CH3OCH3(g)+3H2O(g)ΔH<0。温度升高,该化学平衡移动后到达新的平衡,CH3OCH3的产率将________(填“变大”、“变小”或“不变”,下同),混合气体的平均相对分子质量将_____________________。
Ⅱ.某科研小组欲研究在其他条件不变的情况下,改变起始氧气的物质的量对合成新型硝化剂反应 4NO2(g)+O2(g)![]() 2N2O5(g) ΔH<0的影响。
2N2O5(g) ΔH<0的影响。
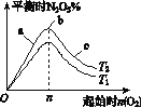
(1)图像中T1和T2的关系是T1________T2(填“>”、“<”或“=”)。
(2)比较a、b、c三点所处的平衡状态中,反应物NO2的转化率最大的是________(填字母)。
【答案】变小 变小 > c
【解析】
Ⅰ.温度升高,化学平衡逆反应方向移动,CH3OCH3的产率变小;逆反应方向气体分子数增加,即气体的物质的量增加,气体质量不变,混合气体的平均相对分子质量将变小;
Ⅱ.(1)①图像中T1→T2时N2O5%增加,平衡向放热的正反应方向移动,应为降温;
(2)O2越多,NO2的转化率越大,以此分析。
Ⅰ.温度升高,化学平衡逆反应方向移动,CH3OCH3的产率变小;逆反应方向气体分子数增加,即气体的物质的量增加,气体质量不变,混合气体的平均相对分子质量将变小;
因此,本题正确答案为:变小;变小;
Ⅱ.(1)①图像中T1→T2时N2O5%增加,平衡向放热的正反应方向移动,应为降温,即T1>T2;
(2)O2越多,则其浓度越大,平衡向正反应方向进行的程度就越大,NO2的转化率越大,故反应物NO2的转化率c>b>a,转化率最大的是c;
因此,本题正确答案为:> ;c。

【题目】“废气”的综合处理与应用技术是科研人员的重要研究课题,CO、SO2、NO2是重要的大气污染气体。
(1)捕集处理后的CO是制取新型能源二甲醚(CH3OCH3)的原料,已知:①CO(g)+H2O(g)![]() CO2(g)+H2(g),△H1=-41.0kJmol-1,②CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H2=-49.0kJmol-1,③CH3OCH2(g)+H2O(g)
CO2(g)+H2(g),△H1=-41.0kJmol-1,②CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H2=-49.0kJmol-1,③CH3OCH2(g)+H2O(g)![]() 2CH3OH(g)△H3=+23.5kJmol-1,则反应2CO(g)+4H2(g)
2CH3OH(g)△H3=+23.5kJmol-1,则反应2CO(g)+4H2(g)![]() CH3OCH2(g)+H2O(g)的△H=______。
CH3OCH2(g)+H2O(g)的△H=______。
(2)采用NaClO2溶液作为吸收剂可对烟气进行脱硝。323K下,向足量碱性NaClO2溶液中通入含NO的烟气,充分反应后,溶液中离子浓度的分析结果如下表,依据表中数据,写出NaClO2溶液脱硝过程中发生的总反应的离子方程式:______。
离子 | NO3- | NO2- | Cl- |
c/(molL-1) | 2.0×10-4 | 1.0×10-4 | 1.75×10-4 |
(3)已知973K时,SO2与NO2反应生成SO3和NO,混合气体经冷凝分离出的SO3可用于制备硫酸。
①973K时测得:NO2(g)![]() NO(g)+1/2O2(g)K1=0.018;SO2(g)1/2+O2(g)SO3(g)K3=20.则反应SO2(g)+NO2(g)
NO(g)+1/2O2(g)K1=0.018;SO2(g)1/2+O2(g)SO3(g)K3=20.则反应SO2(g)+NO2(g)![]() O3(g)+NO(g)的K3=______。
O3(g)+NO(g)的K3=______。
②973K时,向体积为1L的恒容密闭容器中充入SO2、NO2各aml,平衡时SO2的转化率为______。
③恒压下SO2的分压p(SO2)随温度的变化如图所示。当温度升高时,SO2(g)+NO2(g)![]() SO2(g)+NO(g)的化学平衡常数______(填“增大”或”减小”),判断理由是______。
SO2(g)+NO(g)的化学平衡常数______(填“增大”或”减小”),判断理由是______。
(4)用纳米铁可去除污水中的NO3-,反应的离子方程式为4Fe+NO3-+10H+=4Fe2++NH4++3H2O;相同温度下,纳米铁粉去除不同水样中的NO3-的速率有较大差异,下表中Ⅰ和Ⅱ产生差异的原因可能是______;Ⅱ中0~20mim内用NO3-表示的平均反应速率为______molL-1min-1。
反应时间/min | 0 | 10 | 20 | 30 | 40 | |
Ⅰ | c(NO3-)/10-4molL-1 | 8 | 3.2 | 1.6 | 0.8 | 0.64 |
Ⅱ | c(NO3-)/10-4molL-1(含少量Cu2+) | 8 | 0.48 | 0.32 | 0.32 | 0.32 |
【题目】三硫代碳酸钠(Na2CS3)常用作杀菌剂、沉淀剂。某小组设计实验探究三硫代碳酸钠的性质并测定其溶液的浓度。
实验1:探究Na2CS3的性质
步骤 | 操作及现象 |
① | 取少量Na2CS3固体溶于蒸馏水配制成溶液并分成两等份 |
② | 向其中一份溶液中滴加几滴酚酞试液,溶液变红色 |
③ | 向另一份溶液中滴加酸性KMnO4溶液,紫色褪去 |
(1)H2CS3是________酸(填“强”或“弱”)。
(2)已知步骤③的氧化产物是SO42-,写出该反应的离子方程式______
(3)某同学取步骤③所得溶液于试管中,滴加足量盐酸、BaCl2溶液产生白色沉淀,他认为通过测定产生的白色沉淀的质量即可求出实验所用Na2CS3的量,你是否同意他的观点并说明理由______。
实验2:测定Na2CS3溶液的浓度

按如图所示连接好装置,取100mLNa2CS3溶液置于三颈烧瓶中,打开仪器d的活塞,滴入足量2.0mol/L稀H2SO4,关闭活塞。
已知:Na2CS3 + H2SO4=Na2SO4 + CS2 + H2S↑。CS2和H2S均有毒。CS2不溶于水,沸点46℃,与CO2某些性质相似,与NaOH作用生成Na2COS2和H2O。
(4)盛放无水CaCl2的仪器的名称是______,B中发生反应的离子方程式是______。
(5)反应结束后打开活塞k,再缓慢通入热N2一段时间,其目的是______。
(6)为了计算Na2CS3溶液的浓度,对B中混合物进行过滤、洗涤、干燥、称重,得19.2g固体,则A中Na2CS3的物质的量浓度为______。
(7)分析上述实验方案,还可以通过测定C中溶液质量的增加值来计算Na2CS3溶液的浓度,若反应结束后将通热N2改为通热空气,计算值______(填“偏高”、“偏低”或“无影响”)。